(15分)某研究小组设计如下装置分离CO和CO2的混合气体并探究CO还原氧化铜的产物和过氧化钠的性质。已知氯化钯(PdCl2)溶液遇CO气体会产生黑色沉淀(金属单质)。夹持装置未画出。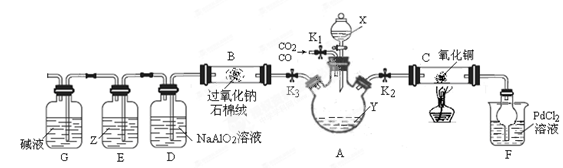
(题9图)
(1)试剂X、Y的焰色反应均呈黄色,则X、Y可能是 、 .
(2)连接装置、检验气密性并装好药品后,关闭分液漏斗活塞和K3,打开K1、K2,分离出CO,当观察到 现象时,可对C装置进行加热操作,反应产物为红色固体。
(3)查询资料获得以下信息:①Cu2O为红色固体;②常温下,Cu2+在溶液中稳定,Cu+易在酸性条件下发生反应:2Cu+ =Cu2++Cu。
甲、乙两组同学取上述红色固体(用M代表)进行实验,探究其成分:
| 组别 | 实验操作 | 实验现象或数据 | 结 论 |
| 甲 | ① 向a g M中加入一定量稀硫酸,充分搅拌; ② 继续滴加稀硫酸至过量, 充分反应. | ①固体明显减少; ②仍然有一定量固体,溶液呈蓝色 | ①M中一定有Cu2O; ②M中一定有Cu. |
| 乙 | 将甲实验后所得溶液过滤 将滤渣洗涤、干燥、称量 | 滤渣质量为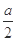 g g | M为Cu和Cu2O的混合物 |
(ii)甲组同学配合乙组同学进行了计算,认为乙组同学的结论是正确的,并得出M中Cu和Cu2O的物质的量之比是 .
(4)C装置反应结束后,欲从混合气体中分离出CO2,需进行的主要操作是 .实验过程中D装置产生白色沉淀的离子方程式为 .
(5)Z试剂为混有KI的苯溶液,则E装置中可能产生的现象是 .
(1)某学习小组利用下图装置制取氯气并探究其性质。
①甲装置中反应的化学方程式是 ;
②证明乙装置中FeCl2溶液与Cl2发生了反应的实验方法是(只注明试剂、现象) ;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是 。
(2)有一瓶长期放置的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究。
试管、胶头滴管、带导管的单孔塞、蒸馏水、1mol·L-1盐酸、品红溶液、新制澄清石灰水。
【提出假设】假设一:该漂白粉未变质,含CaCl2、Ca(ClO)2;
假设二:该漂白粉全部变质,含 ;
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3 。
【进行实验】在答题卡上完成下表(不必检验Ca2+、Cl-):
| 实验步骤 | 预期现象和结论 | |
| ① | 用A试管取少量澄清石灰水备用,用B试管取少量样品,再向B试管 | 若无气体放出且澄清石灰水未见浑浊,则假设一成立; |
| ② | | |
(14分)硒(34Se)和碲(52Te)都是第VIA族元素,硒是分布在地壳中的稀有元素。工业上硒鼓废料(主要成分硒、碲、碳、铜和铁合金)回收精炼硒的流程如下: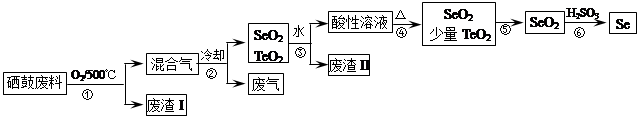
已知:
| 物理性质 | 熔点 | 沸点 | 升华 | 溶解性 |
| SeO2 | 340℃ | 684℃ | 315℃ | 易溶于水 |
| TeO2 | 733℃ | 1260℃ | 450℃ | 微溶于水 |
(2)步骤①中通入的氧气使硒鼓废料翻腾,目的是______。
(3)废气的主要成分是______;废渣II的主要成分是______。
(4)步骤④中主要反应的化学方程式是______;步骤⑥反应的化学方程式是______。
(5)根据表中数据,步骤⑤最适宜的分离方法是______。
沈阳理工大学在废旧电池回收处理现状研究报告中报道了一种湿法处理方法,以下是对废旧电池材料(含有Ni(OH)2、碳粉、氧化铁和铝箔等)进行资源回收所设计的实验流程
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O
③金属离子在该实验流程下完全沉淀的pH:
| 离子 | Al3+ | Fe3+ | Ni2+ |
| pH | 5.2 | 4.1 | 9.7 |
(1)物质A 的作用是调节溶液的pH以除去杂质Fe3+和Al3+,以下最适合作为A物质的是________。
A.NiO B.盐酸 C.NaOH D.氨水
(2)滤渣②的主要成分是_________________________________。
(3)写出加入Na2C2O4溶液反应的化学方程式: _____________。
(4)写出电解滤液③的阴极反应式___________________________。
检验电解滤液③时阳极产生的气体的方法是用湿润的________试纸检验。
(5)由沉淀A生成Ni(OH)3的过程是先在滤渣③中加入过量NaOH溶液进行沉淀转化,待反应完全后再通入电解滤液③产生的气体进行氧化,请写出该氧化过程的离子方程式:__________________。
(6)如何检验Ni(OH)3是否洗涤干净?
________________________________。
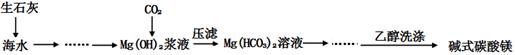
 (x+y)MgO+xCO2↑+(y+z)H2O
(x+y)MgO+xCO2↑+(y+z)H2O
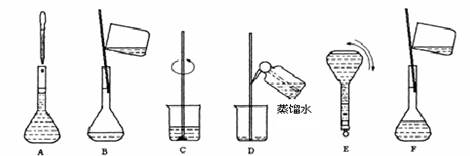
 H2O + CH3CH2—O—CH2CH3 (乙醚)
H2O + CH3CH2—O—CH2CH3 (乙醚)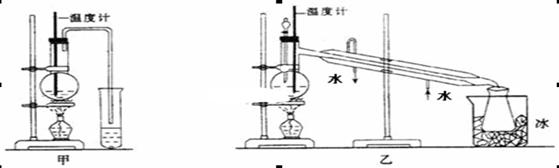

 (3)已知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为 。
(3)已知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为 。