工业上用铝土矿(主要成分为Al2O3,含SiO2、Fe2O3等杂质)为原料冶炼铝的工艺流程如下,对下述流程中的判断正确的是:
| A.试剂X为稀硫酸,沉淀中含有硅的化合物 |
| B.反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
| C.结合质子(H+)的能力由弱到强的顺序是OH->CO32->AlO2- |
| D.Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al |
采用下列装置和操作,能达到实验目的的是
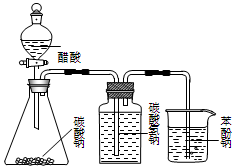


甲 乙 丙 丁
| A.甲装置:加热浓硫酸和乙醇(其体积为比3∶1)混合液,制取乙烯 |
| B.乙装置:比较醋酸、碳酸、苯酚三者的酸性强弱 |
| C.丙装置:向混有苯酚的苯中加入NaOH溶液,除去其中的苯酚 |
| D.丁装置:A中为乙醇、醋酸,B为饱和碳酸钠溶液,制取乙酸乙酯 |
下列说法正确的是
| A.配制100 mL 1.0 mol/L CuSO4溶液,可将25 g CuSO4·5H20溶于100 mL蒸馏水中 |
| B.将几根火柴头浸于水中,一段时间后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素 |
| C.用纸上层析法分离某些物质时,为了看到色斑,只有有色离子的物质才可以用纸层析法 |
| D.减压过滤时,吸滤瓶内液面高度将达到支管口时,应拔掉吸滤瓶上的橡皮管,并从吸滤瓶支管口倒出溶液 |
根据下列实验操作和现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向等浓度且较稀的NaCl、KI混合 液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向溶液x中滴加浓NaOH溶液, 将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中有NH4+ |
| C | 溴乙烷与NaOH溶液共热后,加入 AgNO3溶液 | 未出现淡黄色沉淀 | 溴乙烷没有发生水解 |
| D | 将SO2通入溴水中 | 溴水褪色 | SO2具有还原性 |
下列实验操作不能达到预期实验目的的是
| | 实验目的 | 实验操作 |
| A | 鉴别乙酸乙酯和乙酸 | 分别加入饱和Na2CO3溶液 |
| B | 比较Fe和Cu的金属活动性 | 分别加入浓硝酸 |
| C | 比较H2O和乙醇中羟基氢的活泼性 | 分别加入少量Na |
| D | 比较I2在H2O和CCl4中的溶解度 | 向I2水中加入CCl4,振荡 |
下列有关实验操作,现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将过量CO2通入CaCl2溶液中 | 无白色沉淀 | 生成Ca(HCO3)2溶于水 |
| B | 常温下将Al片插入浓硫酸中 | 无明显现象 | Al片和浓硫酸不反应 |
| C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| D | 将SO2通入溴水中 | 溶液褪色 | SO2具有漂白性 |
下表中的实验操作能达到实验目的或能得出相应结论的是
| 选项 | 实验内容 | 实验目的或实验结论 |
| A | 向盛有2 mL 0.1 mol/L AgNO3溶液的试管中滴加5滴0.1 mol/L NaCl溶液,有白色沉淀生成,再向其中滴加5滴0.1 mol/L KI溶液 | 说明一种沉淀能转化为溶解度更小的沉淀 |
| B | 向1 mL 20% 的蔗糖溶液中加入3~5滴稀硫酸,水浴加热5 min,冷却后再加入新制Cu(OH)2悬浊液,加热 | 证明蔗糖能发生水解反应 |
| C | 水浴加热浓硝酸、浓硫酸和苯的混合物后,直接蒸馏分液后得到的粗产品 | 制备纯硝基苯 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入等体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
下列实验装置或操作正确的是 ( )

| A.实验① 制取氨气 |
| B.实验② 溴水褪色证明了乙烯可以与溴发生加成反应 |
| C.实验③ 比较红磷和白磷的着火点 |
| D.实验④ 用CaC2和饱和食盐水反应制取C2H2 |

