用铁作电极,电解500mL 1mol/L CuCl2溶液,当某电极质量增加19.2g时,停止通电。将溶液转移至蒸发皿中,蒸干灼烧,得到固体质量为
| A.65.1 g | B.40g | C.48.75 g | D.82.7 g |
电化学在日常生活中用途广泛,图①是镁一次氯酸钠燃料电池,电池总反应为:
Mg+ClO—+H2O= Cl—+ Mg(OH)2↓,图②是Cr2O2—7的工业废水的处理。下列说法正确的是
| A.图②中Cr2O2—7离子向惰性电极移动,与该极附近的OH—结合转化成Cr(OH)3除去 |
| B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图①中发生的还原反应是:Mg2++ClO—+ H2O+ 2e—=Cl—+ Mg(OH)2↓ |
| D.若图①中3.6 g镁溶解产生的电量用以图②废水处理,理论可产生10.7 g氢氧化铁沉淀 |
下列四种装置中,溶液的体积均为250 mL,开始时电解质溶液的浓度均为0.10mol/L,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述正确的是
| A.工作一段时间后溶质的物质的量浓度①=②=③=④ |
| B.工作一段时间后溶液的pH:④>③=①>② |
| C.产生气体的总体积:④>②>①>③ |
| D.电极上析出的固体的质量:①>②>③>④ |
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是
| A.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
我国科学家发明的一种可控锂水电池的工作原理如图所示。下列有关说法不正确的是
| A.电池工作时,锂离子向正极移动 |
| B.有机电解质可用水溶液代替 |
| C.电池总反应为2Li + 2H2O="2LiOH" + H2↑ |
| D.该装置不仅可提供电能,还可得到清洁的氢气 |
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应
Cr2O72–+6Fe2++14H+ 2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
A.阳极反应为Fe-2e- Fe2+ Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.反应过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
有一种纸质软电池,该电池采用薄层纸片作为载体和传导体,一面附着锌,另一面附着二氧化锰。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),关于此电池,下列说法正确的是
| A.该电池Zn为负极,ZnO为正极,MnO2催化剂] |
| B.该电池的正极反应为MnO2+e-+H2O=MnO(OH)+OH- |
| C.放电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D.电池工作时OH-通过薄层纸片向附着二氧化锰的电极移动 |
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中,正确的是( )
| A.由TiO2制得1mol 金属Ti ,理论上外电路转移2 mol电子 |
| B.阳极的电极反应式为:C + 2O2-? 4e- ="=" CO2↑ |
| C.在制备金属钛前后,整套装置中CaO的总量减少 |
| D.若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb电极(已知铅蓄电池放电时的总反应为Pb + PbO2 + 2H2SO4= 2PbSO4 + 2H2O) |
发展混合动力车是实施节能减排的重要措施之一。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)电解液。镍氢电池充放电原理总反应式为:H2+2NiOOH 2Ni(OH)2。下列有关混合动力车的判断正确的是:
2Ni(OH)2。下列有关混合动力车的判断正确的是: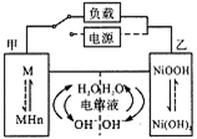
| A.在上坡或加速时,乙电极周围溶液的pH将减小 |
| B.在上坡或加速时,溶液中的K+向甲电极迁移 |
| C.在刹车和下坡时,乙电极增重 |
D.在刹车和下坡时,甲电极的电极反应式为:2H2O+2e- H2↑+2OH- H2↑+2OH- |
