查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH—2e—→X+2H+.下列说法中正确的是( )
| A.电池内部H+由正极向负极移动 |
| B.另一极的电极反应式为:O2+4e—+2H2O=4OH— |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
| D.电池总反应为:2CH3CH2OH + O2→2CH3CHO + 2H2O |
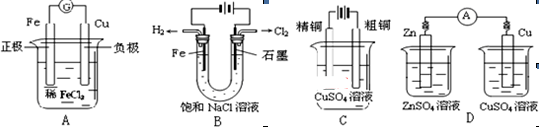
图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法不正确的是

| A.图Ⅰ中a为纯铜 |
| B.图Ⅰ中SO42—向b极移动 |
| C.图Ⅱ中如果a、b间连接电源,则a连接负极 |
| D.图Ⅱ中如果a、b间用导线连接,则X可以是铜 |
如图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是
| A.产生气体的体积:(1)> (2) |
| B.电极上析出物质的质量:(1)> (2) |
| C.溶液pH的变化:(1)增大,(2)减小 |
| D.电极反应式:(1)中阳极:4OH--4e-===2H2O+O2↑,(2)中负极:2H++2e-===H2↑ |
不久前,美国一个海军航空站安装了一 台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600 ℃~700 ℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2=2H2O, 负极反应为H2+ CO32--2e-=H2O+CO2,则下列推断正确的是 ( )
| A.正极反应为:4OH- =O2+2H2O+4e- | B.放电时 CO32-向负极移动 |
| C.电池供应1 mol水蒸气,转移的电子数为4 mol | D.放电时CO32-向正极移动 |
下列关于铜电极的叙述,不正确的是
| A.铜锌原电池中铜是正极 |
| B.用电解法精炼粗铜时,粗铜作阳极 |
| C.在镀件上电镀铜时可用金属铜作阳极 |
| D.电解稀硫酸制H2、O2时,铜作阳极 |
据报道,全球每年发生金属腐蚀而造成的直接经济损失达数千亿美元。下列各电极反应
式中,能表示铁的电化学腐蚀的是
①Fe-2e-=Fe2+
②2H++2e-=H2↑
③Fe-3e-=Fe3+
④2H2O+O2+4e-=4OH-
⑤4OH--4e-=2H2O+O2↑
| A.①②⑤ | B.②③④ | C.①②④ | D.①③⑤ |
有如图装置,下列有关该装置反应开始时的叙述正确的是: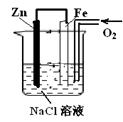
| A.锌极附近滴入酚酞,溶液呈红色。 |
| B.铁极发生的电极反应为:2H2O+O2+4e=4OH- |
| C.铁极发生吸氧腐蚀生成锈蚀 |
| D.溶液中的OH-离子向铁极移动 |
利用如图所示装置可以模拟钢铁的电化学防护。下列说法正确的是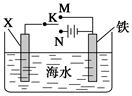
| A.若X为锌棒,开关K置于M处,铁极发生还原反应 |
| B.若X为碳棒,开关K置于N处,X极发生还原反应 |
| C.若X为碳棒,开关K置于N处,可加快铁的腐蚀 |
| D.若X为锌棒,开关K置于M处,可加快铁的腐蚀 |
铜锌原电池(如右图)工作时,下列叙述正确的是
| A.在外电路中,电流从Zn极流向Cu极 |
| B.盐桥中的Cl-移向CuSO4溶液 |
| C.当负极减小65g时,正极增加65g |
| D.电池的总反应为 Zn + Cu2+=Zn2+ + Cu |