题目内容
有如图装置,下列有关该装置反应开始时的叙述正确的是: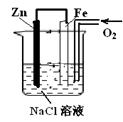
| A.锌极附近滴入酚酞,溶液呈红色。 |
| B.铁极发生的电极反应为:2H2O+O2+4e=4OH- |
| C.铁极发生吸氧腐蚀生成锈蚀 |
| D.溶液中的OH-离子向铁极移动 |
B
解析试题分析:锌比铁活泼,所以锌作负极,铁作正极。该原电池的反应相当于是吸氧腐蚀。A、锌极腐蚀氧化反应,锌失电子成为锌离子进入溶液,所以滴入酚酞,不变红色,错误;B、铁极的氧气发生还原反应,得电子成为氢氧根离子,正确;C、铁极是正极,不发生反应,被保护,错误;D、原电池中阴离子移向负极,所以OH-离子向锌极移动,错误,答案选B。
考点:考查原电池装置的判断,反应原理的应用

X、Y两根金属棒插入Z溶液中构成下图的装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )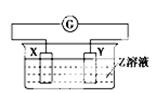
| 编号 | X | Y | Z |
| A | Zn | Cu | 稀硫酸 |
| B | Cu | Zn | 稀硫酸 |
| C | Cu | Ag | 硫酸铜溶液 |
| D | Ag | Zn | 硝酸银溶液 |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见右图,电池总反应可表示为:2H2+O2=2H2O。下列有关说法正确的是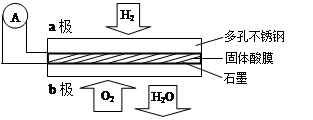
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-=4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法不正确的是

| A.图Ⅰ中a为纯铜 |
| B.图Ⅰ中SO42—向b极移动 |
| C.图Ⅱ中如果a、b间连接电源,则a连接负极 |
| D.图Ⅱ中如果a、b间用导线连接,则X可以是铜 |
汽车的启动电源常用铅蓄电池,电池反应如下:
PbO2 + Pb + 2H2SO4 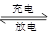 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
| A.PbO2放电时是电池的负极,充电时是电池的阳极。 |
B.负极的电极反应式为:Pb + SO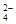 – 2e – = PbSO4 – 2e – = PbSO4 |
| C.放电时,PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
右图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是
| A.电源B端是正极 |
| B.a、c电极均有单质生成,其物质的量之比为2:1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解液为AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |
设计如下装置探究HCl溶液中阴、阳离子在电场中的相对迁移速率(已知:Cd的金属活动性大于Cu)。恒温下,在垂直的玻璃细管内,先放CdCl2溶液及显色剂,然后小心放入HCl溶液,在aa'处形成清晰的界面。通电后,可观察到清晰界面缓缓向上移动。下列说法不正确的是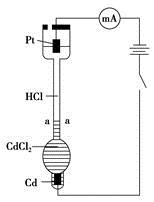
| A.通电后,可观察到清晰界面缓缓向上移动的原因是Cd2+向Pt电极迁移的结果 |
| B.装置中Pt电极附近的pH增大 |
| C.一定时间内,如果通过HCl溶液某一界面的总电量为5.0 C,测得H+所迁移的电量为4.1 C,说明该HCl溶液中H+的迁移速率约是Cl-的4.6倍 |
| D.如果电源正负极反接,则下端产生大量Cl2,使界面不再清晰,实验失败 |
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)
| A.阳极发生还原反应,其电极反应式:Ni2++2e-=Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu和Pt |
科学家们在研制一种吸气式的锂—空气电池,工作时吸收空气中的氧气在多孔金制成的正极表面上反应。总反应可表示为2Li+O2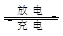 Li2O2,下列有关说法正确的是
Li2O2,下列有关说法正确的是
| A.充电时,多孔金制成的电极外接电源负极 |
| B.放电时,吸收空气中22.4 L的O2,就有2 mol e-从电池负极流出 |
| C.放电时,Li+从负极向正极移动 |
| D.该电池可使用含Li+的水溶液作电解质溶液 |