下列叙述中正确的是
| A.图①中正极附近溶液pH降低 |
| B.图①中电子由Zn流向Cu,盐桥中的Cl—移向CuSO4溶液 |
C.图②正极反应是O2+2H2O+4e¯ 4OH¯ 4OH¯ |
| D.图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
下图是研究铁钉腐蚀的装置图,下列说法不正确的是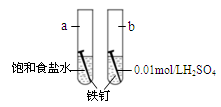
| A.铁钉在两处的腐蚀速率:a < b |
| B.a、b两处铁钉中碳均正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O |
电子表中电源常用银—锌微型电池,电极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH- 电池的总反应式为:Ag2O+Zn= 2Ag+ZnO,下列判断不正确的是
| A.锌为负极,Ag2O为正极 |
| B.锌发生还原反应,氧化银发生氧化反应 |
| C.原电池工作时,负极附近溶液的pH值减小 |
| D.原电池工作时,电子流动方向为Zn→Ag2O |
右图为铜锌原电池示意图,下列说法错误的是( )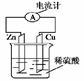
| A.锌片为负极,且逐渐溶解 |
| B.铜片为正极,铜不易失电子而受到保护 |
| C.电子由锌片通过导线流向铜片,H+往铜片运动 |
| D.该装置能将电能转变为化学能 |
用两支惰性电极插入CuSO4溶液中,通电电解,当有1×10-3 mol的OH-放电时,溶液显浅蓝色,则下列叙述正确的是( )
| A.阳极上析出11.2 mL O2(标准状况) | B.阴极上析出32 mg Cu |
| C.阴极上析出11.2 mL H2(标准状况) | D.阳极和阴极质量都无变化 |
下列说法正确的是 ( )
| A.电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e-= Cl2 ↑ |
| B.氢氧燃料电池的负极反应式:O2 + 2H2O+ 4e- ="=" 4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜 |
| D.钢铁发生电化腐蚀的正极反应式:Fe-2e- ="=" Fe2+ |
按下图的装置进行试验,若图中X轴表示阴极的电子的量,则Y轴可能表示为( )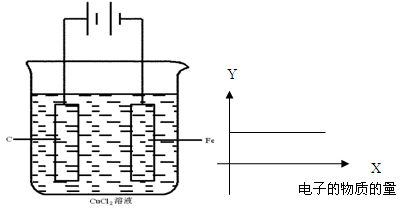
| A.Cu2+物质的量浓度 | B.C棒的质量 |
| C.Fe棒的质量 | D.Cl-物质的量浓度 |
在理论上可用于设计原电池的化学反应是
| A.2Al(s)十2NaOH(aq)+2H2O(1)=2NaAlO2(ag)+3H2(g);△H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(1);△H >0 |
| C.CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);△H <0 |
D.FeCl3(aq)十3H2O(1)  Fe(OH)3(s)+3HCl(aq);△H >0 Fe(OH)3(s)+3HCl(aq);△H >0 |
利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如图所示的循环系统实现光分解水制氢(a、b、c、d均为惰性电极)。反应过程中所需的电能由太阳能光电池提供,反应体系中I2 和Fe3+ 等可循环使用。下列说法正确的是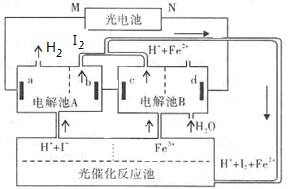
| A.电极M为光电池的正极 |
| B.d的电极反应式为2H2O + 4e- = 4H+ + O2↑ |
C.光催化反应池中反应的离子方程式为2Fe3++ 2I-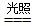 2Fe2+ + I2 2Fe2+ + I2 |
D.若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol·L-1和b mol·L-1,光催化反应生成Fe3+ 的速率为c mol·min-1,则循环系统中溶液的流量为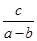 L·mol -1 L·mol -1 |
