如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当电路中通过的电子都是0.1mol时,下列说法正确的是( )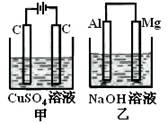
| A.相同条件下产生气体的体积:V甲=V乙 |
| B.溶液pH值变化:甲减小乙增大 |
| C.溶液的质量变化:甲减小乙增大 |
| D.电极反应式:甲中阴极:Cu2++2e—= Cu, 乙中负极:Mg - 2e—= Mg2+ |
铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
| A.因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀 |
| B.若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小 |
| C.铜极上的反应是2H+ + 2e- ="=" H2↑,O2 + 4e- + 4H+ ="=" 2H2O |
| D.在金属表面涂一层油脂,能防止铁铆钉被腐蚀 |
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是
| 待测气体 | 部分电极反应产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
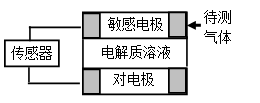
A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为:Cl2 + 2e-= 2Cl-
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
有关下列装置的叙述不正确的是

| A.图①铝片发生的电极反应式是:Al+4OH--3e-===AlO2-+2H2O |
| B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+===Fe2++H2↑ |
| C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| D.图④充电时,阳极反应是:PbSO4+2H2O-2e-===PbO2+SO42-+4H+ |
下列有关电池的说法不正确的是
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.氢氧燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
下列有关说法正确的是
A.氨水稀释后,溶液中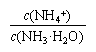 的值减小 的值减小 |
| B.0.1 mol·L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 |
| C.电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 |
| D.298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH>0 |
右图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是
| A.电源B端是正极 |
| B.a、c电极均有单质生成,其物质的量之比为2:1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解液为AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |
下列叙述正确的是
| A.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极区产生的Cl2进入阳极区 |
| B.电解精炼铜时,反应开始一段时间内阳极溶解铜的质量比阴极析出铜的质量大 |
| C.海轮外壳上镶入锌块,可减缓船体的腐蚀 |
| D.在铁片上镀铜时,若铁片增重3.2g,则电路中通过的电子的物质的量为0.05mol |
燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图。下列说法正确的是 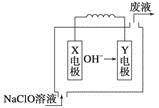
| A.镁作Y电极 |
| B.电池工作时,Na+向负极移动 |
| C.废液的pH大于NaClO溶液的pH |
| D.X电极上发生的反应为ClO-+2H2O-4e-===ClO3-+4H+ |
锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是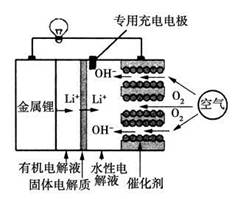
| A.该电池放电时,正极的反应式为O2+4e-+4H+===2H2O |
| B.该电池充电时,阴极发生了氧化反应:Li++e-===Li |
| C.电池中的有机电解液可以用稀盐酸代替 |
| D.正极区产生的LiOH可回收利用 |