下列叙述中,正确的是
①锌跟稀硫酸反应制取氢气,加入少量CuSO4溶液能提高反应速率 ②镀层破损后,白铁(镀锌的铁)比马口铁(铁锡的铁)更易腐蚀; ③电镀时应把镀件置于电解槽的阴极 ;④冶炼铝时,把氧化铝加热成为熔融体后电解 ⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
| A.①②③④⑤ | B.①③④⑤ | C.①③⑤ | D.②④ |
中学教材引入了带盐桥的原电池,该电池即为1806年丹尼尔设计的原电池。如图,下列有关分析正确的是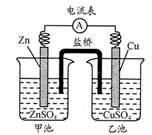
| A.负极发生氧化反应:Cu—2e—=Cu2+ |
| B.电池工作时,盐桥逐渐变蓝 |
| C.向乙池中通入H2S后,电池反应停止 |
| D.若将电极Cu改为石墨,电池电流强度发生变化 |
汽车的启动电源常用铅蓄电池。其结构如下图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O根据此反应判断下列叙述中正确的是
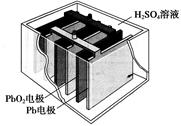
| A.PbO2是电池的负极 |
| B.放电时,溶液中的H+向正极区移动,正极区域的溶液的酸性增强 |
| C.放电时,电子由Pb电极通过导线流向PbO2 |
| D.正极的电极反应式为Pb-2e-=Pb2+ |
上海自主研发了一种氢燃料汽车。它是以30%KOH溶液为电解质的氢氧燃料电池,下列有关说法中,不正确的是( )。
| A.正极反应:O2 + 2H2O + 4e- ="==" 4OH- |
| B.当正极消耗22.4 L H2时,负极11.2 L O2消耗(相同条件) |
| C.发生氧化反应的是负极 |
| D.氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池 |
镍氢电池的总反应为 H2+2NiO(OH) 2Ni(OH)2,根据此反应式判断,此电池放电时,正极上发生反应的物质是( )。
2Ni(OH)2,根据此反应式判断,此电池放电时,正极上发生反应的物质是( )。
| A.NiO(OH) | B.Ni(OH)2 |
| C.H2 | D.H2和NiO(OH) |
下列反应不可用于设计原电池的是( )。
A.2CH3OH+3O2 2CO2+4H2O 2CO2+4H2O |
| B.NaOH+HCl = NaCl+H2O |
| C.Zn+2HCl = ZnCl2+H2↑ |
| D.4Al+3O2+6H2O = 4Al(OH)3 |
下列说法中正确的是
| A.在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率 |
| B.粗铜精炼时,电解液中的c(Cu2+)保持不变 |
| C.Na+的焰色反应呈黄色,属于化学变化 |
| D.在滴定实验中,可以用碱式滴定管量取21.0 mL的NaOH溶液 |
下列关于原电池的叙述中错误的是
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.原电池是将化学能转变为电能的装置 |
| C.在原电池中,电子流出的一极是负极,发生氧化反应 |
| D.原电池放电时,电流的方向是从正极经导线到负极 |
某电化学实验装置如图所示,下列说法正确的是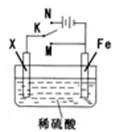
| A.若X为碳棒,开关K置于M处,则溶液中的H+移向Fe极 |
| B.若X为碳棒,开关K置于N处,转移0.2mole一时析出0.lmolO2 |
| C.若X为铜棒,开关K置于M或N处,均可减缓铁的腐蚀 |
| D.若X为锌棒,开关K置于M或N处,锌电极上反应均为Zn-2e一=Zn2+ |
化学家正在研究尿素动力燃料电池,尿液也能发电。用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,下列关于描述正确的是
| A.电池工作时H+ 移向负极 |
| B.该电池用的电解质溶液是KOH溶液 |
| C.甲电极反应式为:CO(NH2 )2 +H2O - 6e-= CO2 +N 2 + 6H+ |
| D.电池工作时,理论每有净化1mol CO(NH2 )2,消耗 33.6 L O2 |