用惰性电极电解某金属元素R的硝酸盐R(NO3)n溶液,通电一段时间后,阳极产生气体V L(标准状况)时,阴极质量增加m g,若R的相对原子质量为M,设NA为阿伏加德罗常数的值,下列叙述中不正确的是
A.电路中通过电子 NA NA | B.n =  |
C.溶液中H+增加 NA NA | D.n = 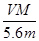 |
如图所示,下列实验现象的描述正确的是
| | a电极 | b电极 | x溶液 | 实 验 现 象 |
| A | 石墨 | 石墨 | CuCl2 | a极质量增加,b极放出无色气体 |
| B | Fe | 石墨 | KNO3 | a极质量增加,b极放出无色气体 |
| C | Fe | Cu | CuSO4 | a极质量增加,b极质量减少 |
| D | 石墨 | 石墨 | HCl | a极放出无色气体,b极放出无色气体 |
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,该溶液放在用惰性电极材料做电极的电解槽中,通电片刻,则氧化产物与还原产物质质量比为…( )
| A.35.5:108 | B.16:207 | C.8:1 | D.108:35.5 |
关于下列各图的说法中,正确的是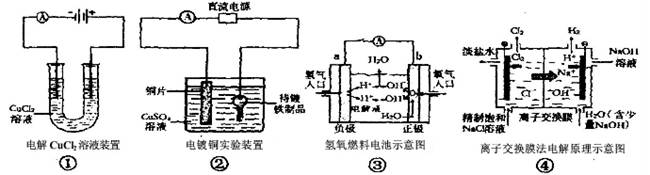
| A.①中与电源负极相连的电极附近能产生使湿润淀粉KI试纸变蓝的气体 |
| B.②中待镀铁制品应该与电源的正极相连接 |
| C.③中的b极是电子流出的极,发生氧化反应 |
| D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
(3分)(2012?山东)下列与金属腐蚀有关的说法正确的是( )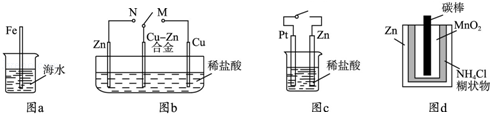
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
(2014?长宁区一模)①②③④甲种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活泼性由大到小的顺序是( )
| A.①③②④ | B.①③④② | C.③④②① | D.③①②④ |
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法正确的是
| A.该装置将电能转化为化学能 |
| B.Li+向a极移动 |
| C.可以用水代替SO(CH3)2做溶剂 |
| D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
下图是模拟电化学反应装置图。下列说法中错误的是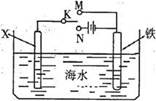
| A.若X为碳棒,开关K置于N处,可以减缓铁的腐蚀 |
| B.若X为锌,开关K置于N处,则X极附近溶液的颜色会变黄色 |
| C.若X为碳棒,开关K置于M处,则X电极的电极反应式为:O2+4e-+2H2O=4OH- |
| D.若X为锌,开关K置于M处,保护铁电极,则为牺牲阳极的阴极保护法 |
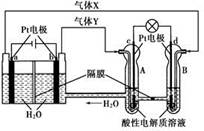
用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是( )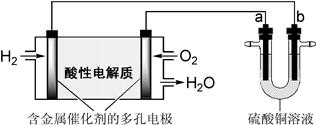
| A.燃料电池工作时,正极反应为:O2+ 2H2O + 4e- ="==" 4OH- |
| B.若a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.若a、b极都是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |