如图是甲醇/过氧化氢燃料电池内部结构示意图。 工作时,甲醇和过氧化氢分别进入燃料电池的燃料腔和氧化剂腔,在各自催化剂的作用下发生反应,并向外界输出电能。下列说法不正确的是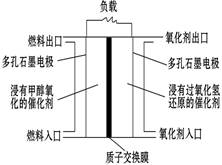
| A.该电池的正极反应式:H2O2+2H++2e—=2H2O |
| B.燃料腔中的多孔石墨电极为该燃料电池的负极,负极产生的H+通过质子交换膜流向正极 |
| C.电池工作时,1 mol甲醇被氧化有6 mol电子转移 |
| D.电路中的电子经正极、负极、质子交换膜后再回到正极,形成闭合回路 |
钛被称为21世纪金属。研究发现,用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图所示装置制备金属钛。下列叙述正确的是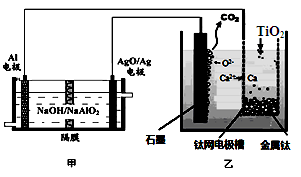
| A.乙装置阴极的电极反应式为 TiO2+4e-=Ti+2O2- |
| B.若不考虑能量的损失,制备24.0g 金属钛,需要消耗金属铝36.0g |
| C.甲装置工作过程中OH-向AgO/Ag极移动;乙装置工作过程中O2-向钛网移动 |
| D.乙装置中的石墨电极需要定期更换 |
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是

A.为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 |
B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
C.电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极 |
| D.此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极 |
某MCFC型燃料电池可同时供应电和水蒸汽,其工作温度为600℃~700℃,所用燃料为氢气,电解质为熔融的K2CO3。该电池的总反应为:2H2+O2=2H2O,负极电极反应式为: H2+CO32——2e— H2O+CO2。则下列判断中正确的是 ( )
H2O+CO2。则下列判断中正确的是 ( )
| A.放电时CO32—向负极移动 | B.放电时CO32—向正极移动 |
| C.正极反应: 4OH——4e—=2H2O+O2↑ | D.当电池中生成1 mol水时,转移4 mol电子 |
高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O===3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述正确的是( )
| A.放电时,负极反应式为3Zn-6e-+6OH-===3Zn(OH)2 |
| B.放电时,正极区溶液的pH减小 |
| C.充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 |
| D.充电时,电池的锌电极接电源的正极 |
锌溴液流电池是一种新型电化学储能装置(如右图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2 + O2 = 2H2O,正极反应为:O2 + 2H2O + 4e- = 4OH-下列叙述不正确的是( )
| A.H2通入负极区 | B.O2通入正极区 |
| C.负极发生氧化反应 | D.正极发生氧化反应 |
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法不正确的是( )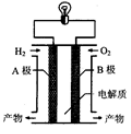
| A.A电极是负极 |
| B.外电路中电子由B电极通过导线流向A电极 |
| C.产物为无污染的水,属于环境友好电池 |
| D.该电池的总反应:2H2+O2===2H2O |
某燃料电池的装置如下图所示,在工作中石墨A电极反应生成一种氧化物Y,下列说法正确的是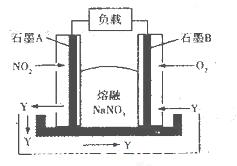
| A.石墨A极为正极,石墨B极为负极 |
| B.Y的化学式可能为NO |
| C.石墨B极上发生氧化反应 |
D.石墨A极的电极反应式为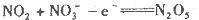 |
镍氢电池比碳锌或碱性电池有更大的输出电流,更适合用于高耗电产品。镍氢电池的总反应式是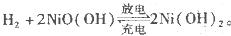 。下列叙述错误的是
。下列叙述错误的是
| A.电池充电时,氢元素被还原 |
| B.电池放电时,镍元素被氧化 |
| C.电池放电时,氢气在负极反应 |
| D.电池放电时,电池负极周围溶液的碱性减弱 |