某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
| A.铜片、铁片、FeCl3溶液组成的原电池 |
| B.石墨、铁片、Fe(NO3)3溶液组成的原电池 |
| C.铁片、锌片、Fe2(SO4)3溶液组成的原电池 |
| D.铜片、铁片、Fe(NO3)3溶液组成的原电池 |
如图装置所示,铜片上发生的反应为
| A.Zn2+ + 2eˉ = Zn |
| B.2H+ + 2eˉ = H2↑ |
| C.Zn - 2eˉ= Zn2+ |
| D.Cu2+ + 2eˉ = Cu |
某MCFC型燃料电池可同时供应电和水蒸汽,其工作温度为600℃~700℃,所用燃料为氢气,电解质为熔融的K2CO3。该电池的总反应为:2H2+O2=2H2O,负极电极反应式为: H2+CO32——2e— H2O+CO2。则下列判断中正确的是
H2O+CO2。则下列判断中正确的是
| A.放电时CO32—向负极移动 |
| B.放电时CO32—向正极移动 |
| C.正极反应: 4OH——4e—=2H2O+O2↑ |
| D.当电池中生成1 mol水时,转移4 mol电子 |
锌片和碳棒用导线连接后插入稀硫酸中,锌片是
| A.阴极 | B.正极 | C.阳极 | D.负极 |
按下图所示装置进行有关实验,则下列叙述正确的是
| A.甲装置用作原电池时,锌为正极 |
| B.甲装置用作原电池时,银棒上发生:Ag+ +e-= Ag |
| C.乙装置用作铜片镀镍时,镍作阴极 |
| D.实现铜片表面镀镍时,可将甲中锌棒与乙中铜片相连,甲中银棒与乙中镍片相连 |
下图为铁、铜水果电池装置示意图,下列说法正确的是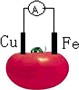
| A.铜片为负极 |
| B.铁片上发生还原反应 |
| C.该装置将电能转变为化学能 |
| D.电子由铁片沿导线流向铜极 |
某同学做完铜、锌稀硫酸原电池的实验后得出了下列结论,你认为正确的是
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.当由铜、锌电极与硫酸铜溶液组成原电池时,铜是负极 |
| C.该实验电子沿导线由锌流向铜,氢离子得到电子而放出氢气 |
| D.铜锌原电池工作时,电流由锌经导线流向铜 |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是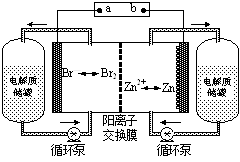
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池。锌电池具有容量大、污染少等优点。电池反应为2Zn+O2=2ZnO,原料为锌粒、电解液和空气。下列叙述正确的是
| A.锌为正极,空气进入负极反应 |
| B.负极反应为Zn+2OH--2e-=ZnO+H2O |
| C.正极发生氧化反应 |
| D.电解液肯定是强酸 |
