题目内容
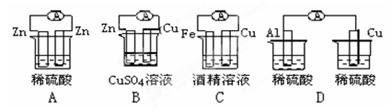
某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
| A.铜片、铁片、FeCl3溶液组成的原电池 |
| B.石墨、铁片、Fe(NO3)3溶液组成的原电池 |
| C.铁片、锌片、Fe2(SO4)3溶液组成的原电池 |
| D.铜片、铁片、Fe(NO3)3溶液组成的原电池 |
C
解析试题分析:某原电池的电池反应为:Fe+2Fe3+===3Fe2+,Fe为负极,做另一电极的金属性比Fe弱,溶液中是电离出Fe3+的盐。故B不能组成该原电池,因为Zn比Fe金属性强。
考点:原电池反应原理与其构成判断。

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
镁―过氧化氢燃料电池具有能量高、安全方便等优点,其结构示意图如图所示。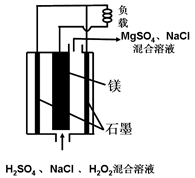
下列有关该电池的叙述中正确的是( )
| A.该电池可以在高温下正常工作 |
| B.电池工作时,正极周围溶液的PH将不断减少 |
| C.电池工作时,H+向负极移动 |
| D.该电池的总反应式为Mg+H2O2+H2SO4=MgSO4+2H2O |
下图为铁、铜水果电池装置示意图,下列说法正确的是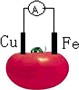
| A.铜片为负极 |
| B.铁片上发生还原反应 |
| C.该装置将电能转变为化学能 |
| D.电子由铁片沿导线流向铜极 |
铜锌原电池(如图)工作时,下列叙述正确的是 ( )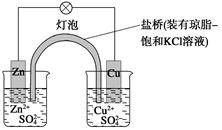
| A.正极反应为:Zn-2e-===Zn2+ |
| B.电池反应为:Zn+Cu2+===Zn2++Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是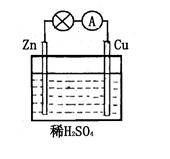
①Zn是负极
②电子由Zn经外电路流向Cu
③Zn极发生氧化反应生成Zn2+
④H+在溶液中由Cu极向Zn极迁移
| A.①②④ | B.②③④ |
| C.①②③ | D.①②③④ |
锂~碘电池可用来为心脏起搏器提供能源,其电池反应可简化为:2Li + I2 = 2LiI。下列有关说法正确的是
| A.I2发生氧化反应 | B.碘电极为该电池的正极 |
C.正极反应为:Li –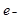 = Li+ = Li+ | D.该电池放电时化学能转化为电能 |
下列对如图所示装置实验判断的描述正确的是( )
| | a电极 | b电极 | X溶液 | 实验判断 |
| A | Cu | Zn | H2SO4 | H+向b极迁移 |
| B | Zn | Fe | H2SO4 | a、b极都放出无色气体 |
| C | Al | Mg | NaOH | a为负极,b为正极 |
| D | Cu | 石墨 | FeCl3 | a极质量减小,b极质量增加 |