对于锌、铜和稀硫酸组成的原电池(如下图),下列有关说法错误的是
| A.溶液中H+向负极移动 | B.电子由Zn经外电路流向Cu |
| C.Zn电极反应:Zn-2e-=Zn2+ | D.Cu是正极 |
下列关于下图所示原电池装置的叙述中,正确的是( ) 
| A.铜片作负极,质量逐渐减小 | B.溶液的pH逐渐减小 |
| C.电流从锌片经导线流向铜片 | D.氢离子在铜片表面被还原 |
原电池产生电流的本质原因是( )
| A.原电池中溶液能电离出自由移动的离子 |
| B.用导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.电极上进行的氧化还原反应中会有电子的转移 |
如下图所示,将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述中正确的是 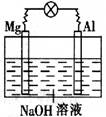
| A.镁比铝活泼,镁失去电子被氧化成Mg2+。 |
| B.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.该装置开始工作时,铝片表面的氧化膜可不必处理 |
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
| A.乙醇在电池的负极上参加反应 |
| B.1mol CH3CH2OH被氧化转移6mol e- |
| C.随着反应的进行,正极附近的酸性减弱。 |
| D.电池正极的电极反应为4H++O2+4e-=2H2O |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是
| A.电池工作时,电子由正极通过外电路流向负极 |
| B.电池工作时,锌失去电子 |
| C.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq) |
| D.外电路中每通过0.2mol e-,锌的质量理论上减小6.5g |
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是
| A.电解时以精铜作阳极 |
| B.电解时阴极发生还原反应 |
| C.粗铜连接电源负极,其电极反应是Cu =Cu2+ + 2e- |
| D.电解结束,电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
某小组为研究电化学原理,设计如图装置。下列叙述错误的是
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动 |
| D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色 |
镁―过氧化氢燃料电池具有能量高、安全方便等优点,其结构示意图如图所示。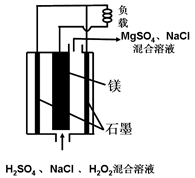
下列有关该电池的叙述中正确的是( )
| A.该电池可以在高温下正常工作 |
| B.电池工作时,正极周围溶液的PH将不断减少 |
| C.电池工作时,H+向负极移动 |
| D.该电池的总反应式为Mg+H2O2+H2SO4=MgSO4+2H2O |