题目内容
某小组为研究电化学原理,设计如图装置。下列叙述错误的是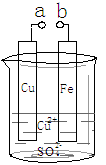
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动 |
| D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色 |
C
解析试题分析:A.a和b不连接时,由于Fe的活动性比Cu强,所以在铁片上发生置换反应,因此会有金属铜析出,正确;B.a和b用导线连接时,就构成了原电池,Fe作负极,Cu作正极,在正极铜片上发生的反应为:Cu2++2e-= Cu,正确;C.a和b分别连接足够电压的直流电源正、负极时,则a是阳极,b是阴极,根据同种电荷相互排斥,异种电荷相互吸引的原则,Cu2+向负电荷较多的铜电极区域移动,错误;D.无论a和b是否用导线连接,铁片均溶解,变为Fe2+, Cu2+则得到电子变为Cu,所以溶液从蓝色逐渐变成浅绿色,正确。
考点:考查原电池、电解池的工作原理的知识。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是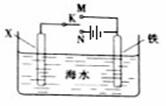
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M处,铁极发生氧化反应 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,X极发生氧化反应 |
下图是锌片和铜片在稀硫酸中所组成的原电池装置,c、d为两个电极。下列有关的判断不正确的是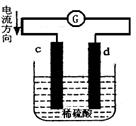
| A.电池工作的过程中,d电极上产生气泡 |
| B.电池工作时,溶液中SO42-向d移动 |
| C.c为负极,发生氧化反应 |
| D.电池工作的过程中,溶液中SO42-浓度基本不变 |
原电池产生电流的本质原因是( )
| A.原电池中溶液能电离出自由移动的离子 |
| B.用导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.电极上进行的氧化还原反应中会有电子的转移 |
下列有关电化学原理的说法错误的是( )
| A.氯化铝的熔点比氧化铝低,因此工业上最好采用电解熔融氯化铝来制备单质铝 |
| B.电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极 |
| C.对于冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法 |
| D.对大型船舶的外壳进行的“牺牲阳极的阴极保护法”,是应用了原电池原理 |
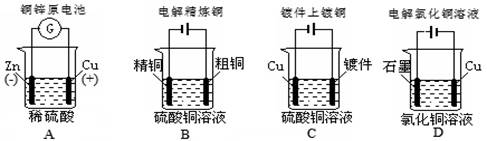
关于下列各装置图的叙述中,不正确的是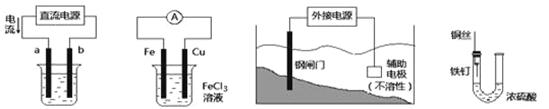
① ② ③ ④
| A.用装置①在铁件上镀铜,则a极为铜,电解质为CuSO4溶液 |
| B.装置②的总反应是:Fe +2Fe3+=3Fe2+ |
| C.装置③中钢闸门应与外接电源的正极相连 |
| D.装置④中的铁钉几乎没被腐蚀 |