Cu—Zn稀硫酸组成原电池装置,当导线中有0.5mol电子通过时,理论上两极的变化是
①锌极反应:Zn-2e-=Zn2+,锌片上产生0.25mol的H2
②铜极反应:2H++2e-=H2↑,锌片溶解16.25g
③电流由铜极经导线流向锌极 ④溶液中SO42-移向铜极
| A.①④ | B.③④ | C.②③ | D.①③ |
如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验: 断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转。下列说法不正确的是
| A.断开K2,闭合K1一段时间,溶液的pH变大 |
| B.断开K1,闭合K2时,b极上的电极反应式为:2H++2e-====H2↑ |
| C.断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-====O2↑+2H2O |
| D.断开K1,闭合K2时,OH-向b极移动 |
用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得的溶液中加入0.1mol Cu2 (OH)2CO3后恰好恢复到电解前的浓度和pH (不考虑二氧化碳的溶解)。则电解过程中转移的电子的物质的量为:
| A.0.4mol | B.0.5mol | C.0.6mol | D.0.8mol |
某原电池的总反应是Zn+Cu2+====Zn2++Cu,则该原电池的组成正确的是( )
| | A | B | C | D |
| 正极 | Zn | Zn | 碳棒 | Cu |
| 负极 | 碳棒 | Fe | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | CuSO4 | ZnCl2 |
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据电镀原理,钢芯镀镍时,钢芯应该做
| A.正极 | B.负极 | C.阳极 | D.阴极 |
关于下图的说法正确的是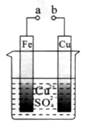
| A.构成原电池时Cu是负极 |
| B.构成电解池时Cu是阴极 |
| C.构成电解池时质量增重的极是阴极 |
D.电池工作时溶液中的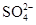 一定移向Cu极 一定移向Cu极 |
如图所示,下列叙述正确的是( ) 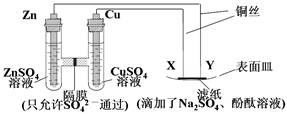
| A.隔膜左侧溶液的质量增加,隔膜右侧溶液的液面升高 |
| B.ZnSO4溶液与CuSO4溶液可以互换 |
| C.X与滤纸接触处有氧气生成 |
| D.Y与滤纸接触处有气泡产生,溶液逐渐变红 |
下列防腐措施中,利用原电池反应使主要金属得到保护的是( )
| A.用氧化剂使金属表面生成致密稳定的氧化物保护膜 |
| B.在金属中加入一些铬或镍制成合金 |
| C.在轮船的壳体水线以下部分装上锌锭 |
| D.金属表面喷漆 |
下图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性。请根据图示判断下列有关说法不正确的是( )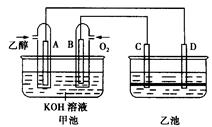
| A.甲池是原电池、乙池是电解池 |
| B.通入乙醇的惰性电极的电极反应式为:C2H5OH+16OH--12e-=2CO32-+11H2O |
| C.反应一段时间后,两池溶液的pH均未变化 |
| D.假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O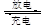 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
有关该电池的说法正确的是( )
| A.充电过程是化学能转化为电能的过程 |
| B.充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
| C.放电时负极附近溶液的碱性增强 |
| D.放电时电解质溶液中的OH-向正极移动 |