题目内容
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据电镀原理,钢芯镀镍时,钢芯应该做
| A.正极 | B.负极 | C.阳极 | D.阴极 |
D
解析试题分析:在电镀时,镀层金属作阳极,镀件作阴极,含有镀层金属的离子的溶液作电镀溶液。我国第五套人民币中的一元硬币材料为钢芯镀镍,依据电镀原理,若在钢芯镀镍时,钢芯应该作阴极。故选项是D。
考点:考查电镀原理的应用的知识。

练习册系列答案
相关题目
某同学用0.10 mol/L的HCl溶液测定未知浓度的NaOH溶液,其实验操作如下:
| A.用酸式滴定管量取20.00 mL HCl溶液注入锥形瓶,同时滴加2-3滴酚酞试液; |
| B.用0.10 mol/L的HC!溶液润洗酸式滴定管; |
| C.把滴定管用蒸馏水洗净; |
| D.取下碱式滴定管,用待测NaOH溶液润洗后,将待测NaOH溶液注入碱式滴定管至距离刻度“0”以上20 cm处,再把碱式滴定管固定好,调节液面; |
F.另取锥形瓶,再重复以上操作1-2次;
G.把锥形瓶放在碱式滴定管下边,瓶下垫一张白纸,边滴边摇动锥形瓶,直到加入最后一滴碱液后溶液颜色突变并在半分钟内不再变色为止,记下滴定管液面所在的刻度。
请回答下列问题:
(1)滴定操作的正确顺序是:(填字母) →C→ →B→ → → 。
(2)G步操作中在锥形瓶下垫一张白纸的作用是 。
(3)D步操作中液面应调节到 ,尖嘴部分应 。
(4)滴定终点读数时,如果仰视液面,读出的数值 ,若滴定前平视读数则由此计算得到的NaOH溶液浓度 (填“偏大”、“偏小”、“无影响”)
(5)如图分别是量筒、滴定管、温度计的一部分,则量筒,滴定管,温度计分别是 (填编号)。

高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是( )。
| A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+ |
| B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
下列事实不能用电化学原理解释的是( )
| A.镀锌铁片比镀锡铁片更耐腐蚀 |
| B.远洋海轮的尾部装上一定数量的锌板 |
| C.常温条件下,在空气中铝不易被腐蚀 |
| D.用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O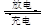 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
有关该电池的说法正确的是( )
| A.充电过程是化学能转化为电能的过程 |
| B.充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
| C.放电时负极附近溶液的碱性增强 |
| D.放电时电解质溶液中的OH-向正极移动 |
燃料电池是燃料(如H2、CO、CH4等)跟氧气或空气起反应,将化学能转变为电能的装置,电解液为强碱溶液。下列关于甲烷燃料电池的说法正确的是( )
| A.负极反应为CH4+10OH-→CO32-+7H2O+8e- |
| B.负极反应为O2+2H2O+4e-→4OH- |
| C.随着放电进行,溶液中的阳离子向负极移动 |
| D.随着放电进行,溶液的PH不变 |
下列说法不正确的是
| A. | B. | C. | D. |
| 通电一段时间后,搅拌均匀,溶液的pH增大 | 甲电极上的电极反应为: 2Cl- -2e- = Cl2↑ | Pt电极上的电极反应为:O2+2H2O+4e-==4OH- | 总反应的离子方程式为: 2Fe3++Cu=Cu2++ 2Fe2+ |
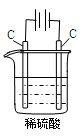 | 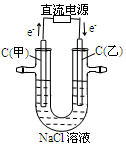 | 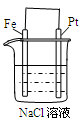 | 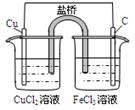 |
对于锌-铜-稀H2SO4组成的原电池装置中,当导线中有1mol电子通过时理论上的电极变化:
①锌片溶解了32.5g ②锌片增重32.5g ③铜片上析出了1g H2 ④铜片上析出1molH2
| A.①③ | B.①④ | C.②③ | D.②④ |
电化学装置工作时,下列电极上发生的反应一定是氧化反应的是( )
| A.阴极 | B.负极 | C.铜电极 | D.石墨电极 |