题目内容
用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得的溶液中加入0.1mol Cu2 (OH)2CO3后恰好恢复到电解前的浓度和pH (不考虑二氧化碳的溶解)。则电解过程中转移的电子的物质的量为:
| A.0.4mol | B.0.5mol | C.0.6mol | D.0.8mol |
C
解析试题分析:由于Cu2(OH) 2CO3+2H2SO4=2CuSO4+3H2O+ CO2↑n(Cu2(OH) 2CO3)= 0.1mol,则根据反应方程式可知产生2mol的CuSO4和3mol的H2O。电解后恰好恢复到电解前的浓度和pH,则电解了0.2mol的CuSO4和0.3mol的H2O。根据电解方程式2CuSO4+3H2O 2Cu+2H2SO4+H2↑+1/2O2↑。则电解过程中转移的电子的物质的量为:0.6mol。因此选项是C。
2Cu+2H2SO4+H2↑+1/2O2↑。则电解过程中转移的电子的物质的量为:0.6mol。因此选项是C。
考点:考查电解原理的应用及有关计算的知识。

某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准盐酸滴定待测的氢氧化钠溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。直到加入一滴盐酸后,溶液颜色由黄色变为橙色,并 为止。
(2)下列操作中可能使所测氢氧化钠溶液的浓度值偏低的是 。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束后俯视读数 |

依据上表数据列式计算该氢氧化钠溶液的物质的量浓度为 。
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法不正确的是
| A.可以用水代替SO(CH3)2做溶剂 | B.电子移动方向是由a极流向b极 |
| C.该装置将化学能转化为电能 | D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
如图,将纯Fe棒和石墨棒插入1 L饱和NaCl溶液中。下列说法正确的是( )
| A.M接负极,N接正极,当两极产生气体总量为22.4 L(标准状况)时,生成1 mol NaOH |
| B.M接负极,N接正极,在溶液中滴人酚酞试液,C电极周围溶液变红 |
| C.M接负极,N接正极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 |
| D.M接电源正极,N接电源负极,将C电极换成Cu电极,电解质溶液换成CuSO4溶液,则可实现在铁上镀铜 |
下列防腐措施中,利用原电池反应使主要金属得到保护的是( )
| A.用氧化剂使金属表面生成致密稳定的氧化物保护膜 |
| B.在金属中加入一些铬或镍制成合金 |
| C.在轮船的壳体水线以下部分装上锌锭 |
| D.金属表面喷漆 |
钢铁发生吸氧腐蚀时,正极发生反应的电极反应式为
| A.Fe-2e-=Fe2+ | B.Fe-3e-=Fe3+ | C.O2+2H2O+4e-=4OH- | D.2H++2e-= H2 ↑ |
在25ºC时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有a mol电子转移时,溶液中析出mg Na2SO4 ·10 H2 O晶体。若温度不变,在剩余溶液中溶质的质量分数为
A.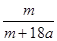 ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D.71m/161(m+9a) ×100% |
一种氢氧燃料电池用30%KOH溶液为电解质溶液,有关这种电池的说法中错误的是
| A.H2在负极发生氧化反应 | B.供电时的总反应为:2H2 + O2 = 2H2O |
| C.产物为无污染的水,属于环境友好电池 | D.负极反应为:H2 - 2e- = 2H+ |
