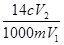某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡常数 Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
Ba2+(aq)+SO42-(aq)的平衡常数 Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
下列叙述正确的是
| A.95 ℃纯水的pH<7,说明加热可导致水呈酸性 |
| B.pH = 3的醋酸溶液,稀释至10倍后pH = 4 |
| C.0.2 mol·L-1的盐酸,与等体积水混合后pH = 1 |
| D.pH = 3的醋酸溶液,与pH = 11的氢氧化钠溶液等体积混合后pH = 7 |
用0.10 mol/L 的盐酸滴定0.10 mol/L 的氨水,滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl ),c(OH ),c(OH )>c(H )>c(H ) ) | B.c(NH4+) = c(Cl ),c(OH ),c(OH ) = c(H ) = c(H ) ) |
C.c(Cl )>c(NH4+),c(OH )>c(NH4+),c(OH )>c(H )>c(H ) ) | D.c(Cl )>c(NH4+),c(H )>c(NH4+),c(H )>c(OH )>c(OH ) ) |
醋酸溶液中存在电离平衡CH3COOH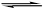 H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
| A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
下列离子方程式中,属于水解反应的是
A.HCOOH+H2O HCOO— + H3O+ HCOO— + H3O+ | B.CO2+H2O HCO3— + H+ HCO3— + H+ |
C.CO32— + H2O HCO3— + OH— HCO3— + OH— | D.HS— + H2O S2— + H3O+ S2— + H3O+ |
酸碱完全中和时
| A.酸和碱的物质的量一定相等 |
| B.酸所提供的H+与碱提供的OH-的物质的量相等 |
| C.酸和碱的物质的量浓度相等 |
| D.溶液一定呈中性 |
下列实验,不能说明乙酸是弱电解质的是
| A.常温时,测得乙酸钠溶液的pH>7 |
| B.常温时,测得0.1 mol·L-1乙酸溶液的pH约为3 |
| C.乙酸溶液与大理石反应产生气泡 |
| D.相同温度下,测得同物质的量浓度的乙酸溶液的导电性比盐酸溶液弱 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是(提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡常数Ksp = c(Ba2+)·c(SO42-),称为溶度积常数。)
Ba2+(aq)+SO42-(aq)的平衡常数Ksp = c(Ba2+)·c(SO42-),称为溶度积常数。)
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.d点无BaSO4沉淀生成 |
| C.通过蒸发可以使溶液由d点变到c点 |
| D.a点对应的Ksp大于c点对应的Ksp |