题目内容
下列实验,不能说明乙酸是弱电解质的是
| A.常温时,测得乙酸钠溶液的pH>7 |
| B.常温时,测得0.1 mol·L-1乙酸溶液的pH约为3 |
| C.乙酸溶液与大理石反应产生气泡 |
| D.相同温度下,测得同物质的量浓度的乙酸溶液的导电性比盐酸溶液弱 |
C
解析试题分析:A、乙酸钠溶液的pH>7 说明乙酸根离子是弱离子水解,正确; B、乙酸部分电离出氢离子,是弱电解质,正确;C、酸的性质,错误;D、导电能力强溶液中离子浓度大,说明乙酸没能完全电离,正确。
考点:考查强弱电解质的判断有关问题。

练习册系列答案
相关题目
从植物的花中可提取一种简写为HIn的有机物,因它在水溶液中存在下列平衡:HIn(红色) H+(无色)+In-(黄色),而被用作酸碱指示剂。往该溶液中加入足量Na2O2粉末,则溶液最终颜色为
H+(无色)+In-(黄色),而被用作酸碱指示剂。往该溶液中加入足量Na2O2粉末,则溶液最终颜色为
| A.红色变深 | B.黄色变浅 | C.黄色变深 | D.褪为无色 |
对于常温下pH为1的硝酸溶液,下列叙述正确的是
| A.该溶液lmL稀释至1000mL后,pH等于3 |
B.该溶液中水电离出的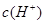 是pH为3的硝酸中水电离出的 是pH为3的硝酸中水电离出的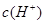 的100倍 的100倍 |
C.该溶液中硝酸电离出的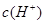 与水电离出的 与水电离出的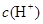 之比值为 之比值为 。 。 |
| D.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 |
W、X、Y、Z是原子序数依次增大的四种短周期元素,化合物WX能抑制水的电离,离子化合物Y2Z能捉进水的电离。则Y元素是
| A.Li | B.F | C.Na | D.Cl |
常温下,pH都等于9的NaOH溶液和CH3COONa两种溶液中,若由水电离产生OH- 浓度分别为a mol/L和b mol/L,则a和b的关系是
| A.a>b | B.a=10-4b | C.b=10-4a | D.a=b |
用0.10 mol/L 的盐酸滴定0.10 mol/L 的氨水,滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl ),c(OH ),c(OH )>c(H )>c(H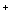 ) ) | B.c(NH4+) = c(Cl ),c(OH ),c(OH ) = c(H ) = c(H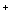 ) ) |
C.c(Cl )>c(NH4+),c(OH )>c(NH4+),c(OH )>c(H )>c(H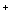 ) ) | D.c(Cl )>c(NH4+),c(H )>c(NH4+),c(H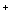 )>c(OH )>c(OH ) ) |
关于强弱电解质的叙述正确的是:( )
| A.强电解质都是离子化合物,弱电解质都是共价化合物 |
| B.强电解质都是可溶性化合物,弱电解质都是难溶性化合物 |
| C.弱电解质的水溶液的导电能力比强电解质溶液弱 |
| D.强电解质的稀溶液中无溶质分子,弱电解质的溶液中存在溶质分子 |
等物质的量浓度的下列四种溶液中, 浓度最大的是( )
浓度最大的是( )
| A.NH4Cl | B.NH4HCO3 | C.NH4NO3 | D.NH4HSO4 |
下列溶液中各微粒的浓度关系正确的是
| A.物质的量浓度相等的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2三种溶液, c (NH4+)的大小顺序为:①>②>③ |
| B.pH相等的NaF与CH3COOK溶液:c(Na+)-c(F —)>c(K+)-c(CH3COO—) |
| C.0.2 mo1·L —1的Na2CO3溶液:c(OH—)=c(HCO3—)+c(H+)+2c(H2CO3) |
| D.0.2 mo1·L —1 HCl与0.1 mo1·L —1 NaAlO2溶液等体积混合:c(Cl—)> c(Na+)>c(Al3+)>c(H+)>c(OH—) |