常温下,体积、物质的量浓度均相等的四种溶液:
①盐酸;②醋酸;③氨水;④CH3COONa溶液。下列说法正确的是
| A.将①与②分别稀释相同倍数后溶液的pH:①>② |
| B.若②与③混合后溶液呈中性,则在常温下Ka(CH3COOH)=Kb(NH3?H2O) |
| C.③与④中已电离的水分子的数目相等 |
| D.②与④混合所得溶液显酸性,则:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
粗制的CuSO4·5H2O晶体中含有Fe2+。提纯时,为了除去Fe2+,常加入少量H2O2, 然后再加入少量碱至溶液pH=4,可以达到除去铁离子而不损失硫酸铜的目的。下列说法不正确的是
| A.溶解CuSO4·5H2O晶体时要加入少量稀H2SO4 |
| B.加入H2O2,将Fe2+氧化,2Fe2+ + H2O2 + 2H+ ="=" 2Fe3+ + 2H2O |
| C.由于CuSO4的催化作用,会使部分H2O2分解而损失 |
| D.调溶液pH=4的依据是Cu(OH)2比Fe(OH)3更难溶 |
硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)  ?[B(OH)4]-(aq)+H+(aq)。下列说法正确的是
?[B(OH)4]-(aq)+H+(aq)。下列说法正确的是
| 化学式 | 电离常数(298 K) |
| H3BO3 | K=5.7×10-10 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| CH3COOH | K=1.75×10-5 |
A.将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生
B.将一滴醋酸溶液滴入碳酸钠溶液中一定能观察到有气泡产生
C.等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者
D.等物质的量浓度的碳酸钠溶液和醋酸钠溶液比较,pH:前者>后者
现有浓度均为0.1mol/L的MgCl2溶液、氨水溶液,按体积比1:2混合。已知Mg(OH)2的Ksp=4.0×10—12,下列说法正确的是
| A.混合前,氨水溶液中c(NH4+):c(OH—)=1:1 |
| B.混合后c(NH4+):c(Cl—)=1:1 |
| C.混合后c(Mg2+)×c(OH—)= 4.0×10—12 |
| D.向混合后的分散系中加入FeCl3溶液,白色沉淀变红褐色 |
25℃时,已知弱酸的电离常数:K(CH3COOH) =" 1.8" ×10-5;K1(H2CO3) =" 4.4" ×10-7;K2(H2CO3) =" 4.7" × 10-11;K(HClO) =" 4.0" ×10-8。则下列说法正确的是
| A.新制氯水与碳酸氢钠不反应 |
| B.25℃时,0.1mol/L的醋酸溶液与0.01mol/L的醋酸溶液中,Ka前者小于后者 |
| C.NaClO溶液中通入少量二氧化碳的反应为:2NaClO+CO2+ H2O = Na2CO3 +2HClO |
| D.等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH |
 )+c(HCO
)+c(HCO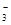 )]
)]