下列说法正确的是
| A.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
| B.0.l0mol·L-1的氨水加水稀释后,溶液中c(NH4+)、c(OH-)变大 |
| C.常温下,向水中加入少量Na2CO3固体后,c(H+)会减小,但Kw不变 |
D.若 LpH=11的NaOH溶液与 LpH=11的NaOH溶液与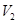 LpH=3的HA溶液混合后显中性,则 LpH=3的HA溶液混合后显中性,则 ≤ ≤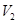 |
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
| A.强酸溶液产生较多的氢气 | B.两者产生等量的氢气 |
| C.无法比较两者产生氢气的量 | D.弱酸溶液产生较多的氢气 |
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少
| A.通入二氧化碳气体 | B.加入氢氧化钠固体 |
| C.通入氯化氢气体 | D.加入饱和石灰水溶液 |
用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是
| A.白醋中滴入石蕊试液呈红色 | B.白醋加入豆浆中有沉淀产生 |
| C.蛋壳浸泡在白醋中有气体放出 | D.pH试纸显示醋酸的pH为2~3 |
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
| A.加入适量的氢氧化钠固体 | B.将溶液稀释到原体积的 10倍 |
| C.加入等体积0.2 mol·L-1氨水 | D.降低溶液的温度 |
在0.1mol·L-1CH3COOH溶液中存在如下电离平衡: CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
| A.加入水时,平衡向生成CH3COOH的方向移动 |
| B.加入少量NaOH固体,平衡向电离的方向移动 |
| C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向电离的方向移动 |
下列图示与对应的叙述相符的是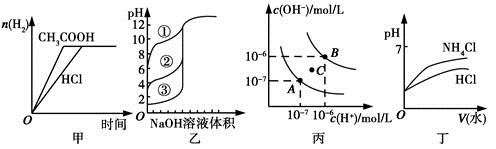
| A.图甲中曲线表示向等体积、等物质的量浓度的盐酸和醋酸溶液中,分别加入足量镁粉,产生H2的物质的量的变化 |
| B.图乙表示用0.1000 mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由曲线可确定③的酸性最强 |
| C.图丙为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
| D.图丁表示将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数时,二者pH的变化 |
已知Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12。在只含有KCl、K2CrO4的混合溶液中滴加0.001 mol·L-1的AgNO3溶液,当AgCl与Ag2CrO4共存时,测得溶液中CrO42-的浓度是5.000×10-3 mol·L-1,此时溶液中Cl-的物质的量浓度是
| A.1.36×10-5 mol·L-1 |
| B.8.90×10-6 mol·L-1 |
| C.4.45×10-2 mol·L-1 |
| D.1×10-5 mol·L-1 |
将一定量下列溶液混合后加热蒸干并灼烧,所得固体不可能为纯净物的是 ( )
| A.FeCl3与FeCl2 | B.KHCO3与KOH | C.NH4Cl与NaCl | D.AlCl3与Al2(SO4)3 |
有0.1 mol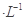 的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
| A.溶液①中,C(CH3COO-)=C(H+) |
| B.溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的C(CH3COO-) |
| C.溶液①、②等体积混合,混合液中c(CH3COO-)+ c(CH3COOH)= C(Na+) |
| D.溶液①、③等体积混合,混合液中C(Na+)>C(CH3COO-)> C(H+)>C(OH-) |