题目内容
有0.1 mol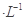 的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
| A.溶液①中,C(CH3COO-)=C(H+) |
| B.溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的C(CH3COO-) |
| C.溶液①、②等体积混合,混合液中c(CH3COO-)+ c(CH3COOH)= C(Na+) |
| D.溶液①、③等体积混合,混合液中C(Na+)>C(CH3COO-)> C(H+)>C(OH-) |
C
解析试题分析:A、溶液①中,醋酸电离产生的C(CH3COO-)=C(H+),但溶液中的C(CH3COO-)<C(H+),错误;B、溶液①、②等体积混合,混合液的CH3COONa的浓度为0.05 mol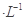 ,所以混合液中c(CH3COO-)小于溶液③中的C(CH3COO-),错误;C、溶液①、②等体积混合,混合液的CH3COONa的浓度为0.05 mol
,所以混合液中c(CH3COO-)小于溶液③中的C(CH3COO-),错误;C、溶液①、②等体积混合,混合液的CH3COONa的浓度为0.05 mol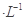 ,根据物料守恒规律,有c(CH3COO-)+ c(CH3COOH)= C(Na+)="0.05" mol
,根据物料守恒规律,有c(CH3COO-)+ c(CH3COOH)= C(Na+)="0.05" mol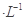 ,正确;D、溶液①、③等体积混合,溶液为酸性,所以C(CH3COO-)> C(Na+),错误,答案选C。
,正确;D、溶液①、③等体积混合,溶液为酸性,所以C(CH3COO-)> C(Na+),错误,答案选C。
考点:考查混合液中的离子浓度的大小比较,守恒规律的应用

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是
| A.HA为一元强酸 |
| B.N点水的电离程度小于K点水的电离程度 |
C.随着MOH溶液的滴加,比值 不变 不变 |
| D.若K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L |
某混合溶液中所含离子的浓度如下表,则M离子可能为
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度 /(mol·L-1) | 2 | 1 | 2 | 1 |
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
| A.加入适量的氢氧化钠固体 | B.将溶液稀释到原体积的 10倍 |
| C.加入等体积0.2 mol·L-1氨水 | D.降低溶液的温度 |
常温下,将0.01 mol·L-1 Na2SO3溶液与0.01 mol·L-1 KHSO3溶液等体积混合,若忽略混合后溶液的体积的变化,则下列判断正确的量( )
| A.混合后溶液中存在有关系:C(K+)+C(Na+)+C(H+)=C(SO32-)+C(HSO3-)+C(OH-) |
| B.混合后溶液中存在有关系:C(K+)+C(H2SO3)+C(H+)=C(SO32-)+C(OH-) |
| C.混合后溶液中存在有关系:C(SO32-)+C(HSO3-)+C(H2SO3)=0.02 mol/L |
| D.两溶液混合前,Na2SO3溶液中,水电离出C(H+)小于KHSO3溶液中水电离出C(H+) |
硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)  ?[B(OH)4]-(aq)+H+(aq)。下列说法正确的是
?[B(OH)4]-(aq)+H+(aq)。下列说法正确的是
| 化学式 | 电离常数(298 K) |
| H3BO3 | K=5.7×10-10 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| CH3COOH | K=1.75×10-5 |
A.将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生
B.将一滴醋酸溶液滴入碳酸钠溶液中一定能观察到有气泡产生
C.等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者
D.等物质的量浓度的碳酸钠溶液和醋酸钠溶液比较,pH:前者>后者
下列实验不能达到目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向5 mL 0.1 mol/L AgNO3溶液中滴加3滴0.1 mol/LNaCl溶液,产生白色沉淀;再向其中滴加3滴0.1mol/L的KI溶液,有黄色沉淀产生 | 验证Ksp(AgCl)> Ksp(AgI) |
| B | 向适量样品溶液中滴加KSCN溶液 | 检验FeSO4溶液是否被氧化 |
| C | 向适量样品溶液中滴加盐酸酸化,再滴加BaCl2溶液 | 检验Na2SO3溶液是否被氧化 |
| D | 向Na2SiO3溶液中通入CO2 | 验证非金属性:碳>硅 |
下列实验操作不能达到其对应目的的是
| 序号 | 实验内容 | 实验目的 |
| A. | 向盛有10滴0.1 mol/L AgNO3溶液的试管中滴加0.1 mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
| B. | 向2 mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
| C. | 向Na2SiO3溶液中通入CO2 | 证明碳酸的酸性比硅酸强 |
| D. | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热 | 验证淀粉已水解 |