题目内容
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少
| A.通入二氧化碳气体 | B.加入氢氧化钠固体 |
| C.通入氯化氢气体 | D.加入饱和石灰水溶液 |
D
解析试题分析:在NaHCO3溶液中存在电离平衡:HCO3- CO32-+ H+。A.通入二氧化碳气体,会发生反应:CO2+ CO32-+H2O="2" HCO3-;所以c(CO32-)会减小,c(HCO3-)会增大。错误。B.加入氢氧化钠固体,由于OH-会中和H+,使c(H+)减小,电离平衡正向移动,c(CO32-)增大,c(HCO3-)减小,不符合题意。错误。C.通入氯化氢气体,HCl溶于水,电离产生H+,使溶液中的c(H+)增大,电离平衡逆向移动,c(CO32-)减小,c(HCO3-)增大,不符合题意。错误。D.加入饱和石灰水溶液,会发生反应:Ca(OH)2+ NaHCO3=CaCO3↓+NaOH+H2O,溶液中c(H+)、c(CO32-)、c(HCO3-)都减少.符合题意。正确。
CO32-+ H+。A.通入二氧化碳气体,会发生反应:CO2+ CO32-+H2O="2" HCO3-;所以c(CO32-)会减小,c(HCO3-)会增大。错误。B.加入氢氧化钠固体,由于OH-会中和H+,使c(H+)减小,电离平衡正向移动,c(CO32-)增大,c(HCO3-)减小,不符合题意。错误。C.通入氯化氢气体,HCl溶于水,电离产生H+,使溶液中的c(H+)增大,电离平衡逆向移动,c(CO32-)减小,c(HCO3-)增大,不符合题意。错误。D.加入饱和石灰水溶液,会发生反应:Ca(OH)2+ NaHCO3=CaCO3↓+NaOH+H2O,溶液中c(H+)、c(CO32-)、c(HCO3-)都减少.符合题意。正确。
考点:考查弱酸的酸式盐的电离平衡的影响因素的知识。

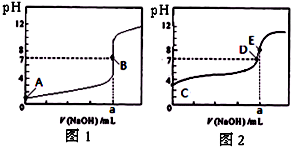
25℃时,向20.00mLNaOH溶液中逐滴加入0.20mo1·L-l的CH3COOH溶液得到如图曲线。下列说法正确的是
| A.水电离出的氢离子浓度:a>b |
| B.c点时恰好中和 |
| C.在d~e之间存在如下关系:C(Na十)>c(CH3COO-)>c(H十)>c(OH一) |
| D.e点时溶液中溶质是CH3COONa和CH3COOH |
某混合溶液中所含离子的浓度如下表,则M离子可能为
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度 /(mol·L-1) | 2 | 1 | 2 | 1 |
常温下,pH=12的NaOH溶液和pH=2的醋酸混合后恰好完全反应(不考虑溶液体积的变化)。下列说法正确的是
| A.反应后的溶液呈酸性 |
| B.两种反应物中水电离出的c(H+)都是1×10-12 mol·L-1 |
| C.反应后的溶液中:c(CH3COO-)+c(CH3COOH)=0.01mol·L-1 |
| D.反应后的溶液中:c(Na+) >c(CH3COO-)>c( OH-)>c(H+) |
醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
| A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
已知Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12。在只含有KCl、K2CrO4的混合溶液中滴加0.001 mol·L-1的AgNO3溶液,当AgCl与Ag2CrO4共存时,测得溶液中CrO42-的浓度是5.000×10-3 mol·L-1,此时溶液中Cl-的物质的量浓度是
| A.1.36×10-5 mol·L-1 |
| B.8.90×10-6 mol·L-1 |
| C.4.45×10-2 mol·L-1 |
| D.1×10-5 mol·L-1 |
硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)  ?[B(OH)4]-(aq)+H+(aq)。下列说法正确的是
?[B(OH)4]-(aq)+H+(aq)。下列说法正确的是
| 化学式 | 电离常数(298 K) |
| H3BO3 | K=5.7×10-10 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| CH3COOH | K=1.75×10-5 |
A.将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生
B.将一滴醋酸溶液滴入碳酸钠溶液中一定能观察到有气泡产生
C.等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者
D.等物质的量浓度的碳酸钠溶液和醋酸钠溶液比较,pH:前者>后者