常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是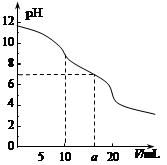
| A.当V=0时:c(H+)+c(HCO 3-)+c(H2CO3)=c(OH-) |
| B.当V=5时:c(CO32—)+c(HCO 3-)+c(H2CO3)=2c(Cl-) |
| C.当V=10时:c(Na+)>c(HCO 3-)>c(CO32—)>c(H2CO3)[来源:学*科*网] |
| D.当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |
下列叙述正确的是
| A.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
B.2SO2(g) + O2(g) 2SO3(g)的正、逆反应的平衡常数K随温度的变化可用上图表示 2SO3(g)的正、逆反应的平衡常数K随温度的变化可用上图表示 |
C.2NO+2CO 2CO2+N2的ΔH<0,常温下该反应一定能自发进行 2CO2+N2的ΔH<0,常温下该反应一定能自发进行 |
| D.25°C时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)减小 |
下列事实能说明NH3·H2O一定是弱电解质的是
①常温下,NH3·H2O溶液能使酚酞变红; ②用NH3·H2O溶液做导电性实验,灯泡很暗;
③常温下,0.1mol / L氯化铵溶液的pH约为5
④常温下,体积相同且pH相同的NH3·H2O溶液和NaOH溶液,与相同浓度的HCl溶液中和时,消耗HCl溶液的体积:前者>后者
| A.①②③④ | B.②③④ | C.③④ | D.②④ |
一定温度下,满足下列条件的溶液一定呈酸性的是
| A.pH=6的某溶液 | B.加酚酞后显无色的溶液 |
| C.能与金属Al反应放出H2的溶液 | D.c(H+)>c(OH—)的任意水溶液 |
已知KHSO3溶液呈弱酸性。在0.1mol·L-1KHSO3溶液中,下列关系正确的是
| A.c(K+)+ c(H+) =c(HSO3-)+ c(OH-)+ c(SO32-) |
| B.c(HSO3-) + c(SO32-) = 0.1mol·L-1 |
| C.c(SO32-) < c(H2SO3) |
| D.c(K+) = c(H2SO3) + c(HSO3-) + c(SO32-) |
已知:CaC2O4沉淀的Ksp=2.3×10-9,将等体积的CaCl2溶液与Na2C2O4溶液混合,若起始CaCl2的浓度为1×10-2mo1·L-1,则生成沉淀所需Na2C2O4溶液的最小起始浓度为
| A.2. 3×10-7mol·L-1 | B.4. 6×10-7mol·L-1 |
| C.9. 2×10-7mol·L-1 | D. ×10-3mol·L-1 ×10-3mol·L-1 |
为了除去MgCl2酸性溶液中的 Fe3+,可在加热搅拌条件下加入一种试剂,过滤后,在向滤液中加入适量的盐酸,这种试剂是
| A.NaOH | B.NH3·H2O | C.MgCl2 | D.MgCO3 |
已知室温时,0.1mo1/LCH3COOH在水中有0.1%发生电离,下列叙述正确的是:
| A.该溶液的pH=5 |
| B.由CH3COOH电离出的c(H+)约为水电离出的c(H+)的106倍 |
C.CH3COOH的电离平衡常数约为1×10-6 |
| D.升高温度,溶液的pH增大 |
下列液体均处于25℃,有关叙述正确的是
| A.某物质的溶液pH <7,则该物质一定是酸或强酸弱碱盐 |
| B.用广泛pH试纸测得0.10 mol·L-1 NH4Cl溶液的pH=5. 2 |
| C.pH=2的CH3COOH中c(H+)是pH=1的CH3COOH中c(H+)的2倍 |
| D.AgCl在相同物质的量浓度的CaCl2和HCl溶液中的Ksp相同 |