题目内容
一定温度下,满足下列条件的溶液一定呈酸性的是
| A.pH=6的某溶液 | B.加酚酞后显无色的溶液 |
| C.能与金属Al反应放出H2的溶液 | D.c(H+)>c(OH—)的任意水溶液 |
D
解析试题分析:A、当温度升高时,水的离子积增大,[H+]=[OH-]=10-6mol/L,此时溶液仍呈中性,故A错误;酚酞的变色范围是8-10,小于8时溶液显无色,可能为碱性、中性或酸性,故B错误;C、能与铝作用放出氢气的可能为强酸或强碱,故C错误;溶液的酸碱性决定于氢离子和氢氧根离子浓度的相对大小,当氢离子的浓度大于氢氧根离子的浓度时,溶液一定呈酸性,D正确;故选D。
考点:溶液酸碱性的判断。

练习册系列答案
相关题目
已知:常温下浓度为0.1 mol·L-1的下列溶液的pH如表:
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B.若将CO2通入0.1 mol·L-1Na2CO3溶液中至溶液中性,则溶液中
2 c (CO32ˉ)+ c (HCO3ˉ)=" 0.1" mol·L-1
C.根据上表,水解方程式ClOˉ+ H2O
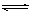 HClO + OHˉ的平衡常数K≈10ˉ7.6
HClO + OHˉ的平衡常数K≈10ˉ7.6D.向上述NaClO 溶液中通HF气体至恰好完全反应时:
c(Na+)>c(Fˉ)>c(H+)>c(HClO)>c(OHˉ)
下列过程表达式中,属于电离方程式的是
A.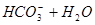  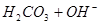 | B.  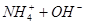 |
C.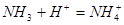 | D.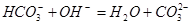 |
下列说法正确的是
| A.向蒸馏水中滴加浓H2SO4时,KW不变 |
| B.常温下,0.005mol·L-1Ba(OH)2溶液pH为12 |
C.Na2CO3水解的离子方程式为:CO32- + 2H2O H2CO3+ 2OH- H2CO3+ 2OH- |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
已知室温时,0.1mo1/LCH3COOH在水中有0.1%发生电离,下列叙述正确的是:
| A.该溶液的pH=5 |
| B.由CH3COOH电离出的c(H+)约为水电离出的c(H+)的106倍 |
C.CH3COOH的电离平衡常数约为1×10-6 |
| D.升高温度,溶液的pH增大 |
下列溶液中各微粒的浓度关系正确的是
| A.物质的量浓度相等的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2三种溶液, c (NH4+)的大小顺序为:①>②>③ |
| B.pH相等的NaF与CH3COOK溶液:c(Na+)-c(F —)>c(K+)-c(CH3COO—) |
| C.0.2 mo1·L —1的Na2CO3溶液:c(OH—)=c(HCO3—)+c(H+)+2c(H2CO3) |
D.0.2 mo1·L —1 HCl与0.1 mo1·L —1 NaAlO2溶N液等体积混合: c(Cl—)> c(Na+)>c(Al3+)>c(H+)>c(OH—) c(Cl—)> c(Na+)>c(Al3+)>c(H+)>c(OH—) |
常温时,下列叙述正确的是
| A.pH=9的NH4Cl与NH3?H2O混合溶液中c(Cl-)>c(NH4+) |
| B.pH=2.5的可乐中c(H+) 是pH=3.5的柠檬水中c(H+)的10倍 |
| C.AgCl在0.1mol /L CaCl2溶液和0.1mol/L NaCl溶液中的溶解度相同 |
| D.1 mL 1mol /L Na2CO3溶液加水稀释至100mL, pH和Kw均减小 |
在100mL0.1mol/L醋酸溶液中加入以下物质中的一种,醋酸溶液pH变小。所加入的这种物质是
| A.水 | B.0.1mol/L盐酸 |
| C.醋酸钠晶体 | D.0.1mol/L氢氧化钠溶液 |
室温下,对pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,其中叙述正确的是
| A.温度升高20℃后,两溶液pH均不变 |
| B.加适量的醋酸钠晶体后,两溶液的pH均增大 |
| C.加水稀释2倍后,两溶液的pH同等程度减小 |
| D.加足量的锌充分反应后,两溶液中产生的氢气一样多 |