将反应Cu (s) + 2Ag+ (aq)  Cu2+ (aq) + 2Ag (s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是
Cu2+ (aq) + 2Ag (s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是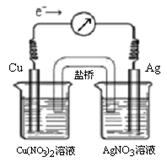
| A.KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B.当电流计指针为0时,该反应达平衡,平衡常数K=0 |
| C.若此时向AgNO3溶液中加入NaCl固体,随着NaCl量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转 |
| D.若此时向Cu(NO3)2溶液中加入NaOH固体,随着NaOH量的增加电流计指针向右偏转幅度减小→指针指向0→向左偏转 |
在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g) CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如下图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如下图所示,下列说法正确的是
A.平衡常数K= |
| B.该反应在T1时的平衡常数比T2时的小 |
| C.任意时刻,T2温度下的反应速率均大于T1温度下的速率 |
D.处于A点的反应体系从T1变到T2,达到平衡时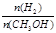 增大 增大 |
某温度下,把3molA和2.5molB混合,盛入容积为2L的容器内,使它们发生反应:
3A(气)+B(气) xC(气)+2D(气)
xC(气)+2D(气)
经过5min后达到平衡生成1mol D , 测得C的平均生成速率为0.10mol·L-1·min-1。下列叙述不正确的是
| A.x的值为2 |
| B.B的转化率为20% |
| C.平衡常数为1/3 |
| D.A的平均消耗速率为0.15mol·L-1·min-1 |
一定量的锌粒与足量稀硫酸反应,向反应混合液中加入某些物质,下列判断正确的是
| A.加入少量水,产生H速率减小,H2体积不变 |
| B.加入NH4HSO4固体,产生H2速率不变,H2体积不变 |
| C.加入CH3COONa固体,产生H2速率减小,H2体积减小 |
| D.滴加少量CuSO4溶液,产生H2速率变大,H2体积减小 |
工业上采用乙烯和水蒸气合成乙醇的原理为:CH2=CH2(g) + H2O(g)  CH3CH2OH(g)。下图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是( )
CH3CH2OH(g)。下图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是( )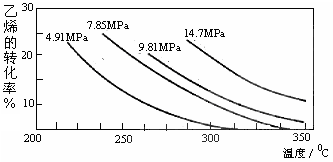
| A.该反应为吸热反应 |
| B.工业上采用7MPa左右,250~300℃,是综合考虑反应速率和乙醇的产率等因素的结果 |
| C.相同温度下,压强越大,乙烯的转化率越大,平衡常数越大 |
| D.给予足够的压强和适当的温度,可实现乙烯的转化率为 100% |
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:
PCl3(g)+ Cl2(g)? PCl5(g);5min末达到平衡,有关数据如右表。
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度(mol?L—1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol?L—1) | C1 | C2 | 0.4 |
下列判断不正确的是
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5min内,v(PCl3)="0.08" mol?L-1?min-1
C.当容器中为1.2mol时,可逆反应达到平衡状态
D.平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol?L—1
某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图Ⅱ所示。则下列结论正确的是
| A.该反应的热化学方程式为:ΔH>0 |
| B.若其它条件不变,升高温度,正、逆反应速率均增大,X的转化率减小 |
| C.达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动 |
| D.达到平衡后,若其他条件不变,通人稀有气体,平衡向正反应方向移动 |
某可逆反应平衡常数表达式为 。达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是( )
。达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是( )
A.反应的热化学方程式为NO2(g)+SO2(g)  NO(g)+SO3(g) ΔH>0 NO(g)+SO3(g) ΔH>0 |
| B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深 |
| C.混合气体的平均摩尔质量保持不变,说明反应已达平衡 |
| D.使用合适的催化剂可使该反应的反应速率和平衡常数增大 |
在一密闭容器中发生可逆反应2A(g)+B(g)  2C(g),下表为反应在不同压强和温度下物质A的平衡转化率,有关说法正确的是( )
2C(g),下表为反应在不同压强和温度下物质A的平衡转化率,有关说法正确的是( )
 A转化率 压强 A转化率 压强温度 | P1(Mpa) | P2(Mpa) |
| 400℃ | 99.6% | 99.7% |
| 500℃ | 96.9% | 97.8% |
A.物质B可以是气态,也可以是非气态
B.P1>P2
C.该反应为吸热反应
D.若反应在恒压为B,初始温度为400℃下的绝热密闭容器中进行,平衡时A的转化率小于0.996
 B(g)+C(g);ΔH ="-48.25" kJ · mol-1反应过程中时间t与A 、B浓度有下图所示关系,若测得第15min时c(B)="1.6" mol·L-1,则下列结论正确的是
B(g)+C(g);ΔH ="-48.25" kJ · mol-1反应过程中时间t与A 、B浓度有下图所示关系,若测得第15min时c(B)="1.6" mol·L-1,则下列结论正确的是