升高温度,下列数据不一定增大的是( )
| A.化学反应速率v | B.化学平衡常数K |
| C.水的离子积常数Kw | D.弱酸的电离常数Ka |
下列对于化学反应方向说法正确的是 ( )
| A.反应2A(g)+B(g) =" 3C" (s)+D(g)在一定条件下能自发进行,说明该反应的ΔH>0 |
| B.常温下反应2Na2SO3(s)+O2(g)= 2Na2SO4(s)能自发进行,则ΔH<0 |
C.反应2Mg(s)+CO2(g) C(s)+2MgO(s)能自发进行,则该反应的△H>0 C(s)+2MgO(s)能自发进行,则该反应的△H>0 |
| D.一定温度下,反应2NaCl(s)=2Na(s)+Cl2(g)的 △H<0 ,△S>0 |
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 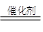 2CO2(g)+S(l) ΔH<0
2CO2(g)+S(l) ΔH<0
若反应在恒容的密闭容器中进行,下列有关说法正确的是
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
下列说法正确的是
| A.增大体系压强,活化分子数增加,化学反应速率一定增大 |
| B.加入反应物,使活化分子百分数增加,化学反应速率增大 |
| C.活化分子间所发生的分子间的碰撞均为有效碰撞 |
| D.升高温度,活化分子百分数增加,化学反应速率一定增大 |
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:
CO(g)+ H2O(g) CO2(g) + H2(g) △H <0
CO2(g) + H2(g) △H <0
反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增加压强 | B.降低温度 | C.增大CO 的浓度 | D.更换催化剂 |
COCl2(g) CO(g)+Cl2(g); △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g); △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
在一定温度下,向容积不变的密闭容器中充入amolA,发生反应:2A(g) B(g);△H<0。达平衡后再向容器中充入amolA,再次达到平衡后,与原平衡比较,下列叙述不正确的是
| A.相对平均分子质量增大 |
| B.A的转化提高 |
C.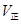 增大, 增大, 减小 减小 |
| D.反应放出的总热量大于原来的2倍 |
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面 合成乙醇,反应原理为:
CH2=CH2(g)+H2O(g)  CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是
| A.合成乙醇的反应一定为吸热反应 |
| B.目前工业上釆用250?300℃,主要是在此温度下乙烯的转化率最大 |
| C.目前工业上采用加压条件(7MPa左右),目的是提高乙醇的产率和加快反应速率 |
| D.相同催化剂下,在300℃14.7MPa乙醇产率反而比300℃7MPa低得多,是因为加压平衡向逆反应方向移动 |
已知:2SO2(g)+O2(g) 2SO3(g) △H=—196.6kJ·mol—1,向密闭容器中加入2mol SO2(g)和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是
2SO3(g) △H=—196.6kJ·mol—1,向密闭容器中加入2mol SO2(g)和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是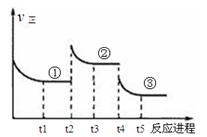
注:t1~t2、t3~t4、t5之后各时间段表示达到平衡状态①、②、③。
| A.t2~t3时间段,平衡向逆反应方向移动 |
| B.平衡状态①和②,平衡常数K值相同 |
| C.平衡状态①和②,SO2转化率相同 |
| D.t4时刻改变的条件是减小压强 |
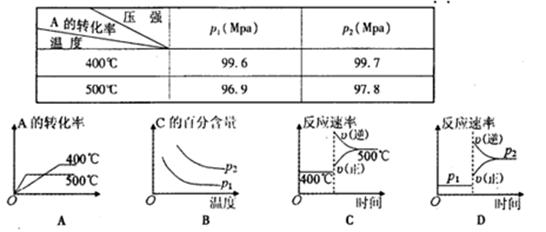
 2C(g),根据下表中的数据判断下列图像错误的是
2C(g),根据下表中的数据判断下列图像错误的是