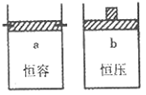
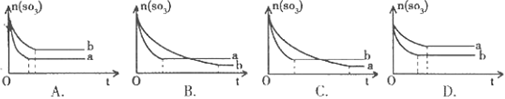
��Ŀ����
��֪��2SO2(g)+O2(g) 2SO3(g) ��H����196.6kJ��mol��1�����ܱ������м���2mol SO2(g)��1mol O2��һ�������·�Ӧ�ﵽƽ�⣬��t2��t4ʱ�̷ֱ�ֻ�ı�һ���������¶Ȼ�ѹǿ������Ӧ����������Ӧ��������ͼ��ʾ������˵����ȷ����
2SO3(g) ��H����196.6kJ��mol��1�����ܱ������м���2mol SO2(g)��1mol O2��һ�������·�Ӧ�ﵽƽ�⣬��t2��t4ʱ�̷ֱ�ֻ�ı�һ���������¶Ȼ�ѹǿ������Ӧ����������Ӧ��������ͼ��ʾ������˵����ȷ����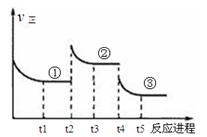
ע��t1��t2��t3��t4��t5֮���ʱ��α�ʾ�ﵽƽ��״̬�١��ڡ��ۡ�
| A��t2��t3ʱ��Σ�ƽ�����淴Ӧ�����ƶ� |
| B��ƽ��״̬�ٺ͢ڣ�ƽ�ⳣ��Kֵ��ͬ |
| C��ƽ��״̬�ٺ͢ڣ�SO2ת������ͬ |
| D��t4ʱ�̸ı�������Ǽ�Сѹǿ |
B
�������������A�t2ʱ����˲�������С��ƽ��״̬������ƽ��������Ӧ�����ƶ���B�ƽ��״̬�ٱ�Ϊ����v��˲�����֪�����������¶Ⱥ�����ѹǿ���£��������¶ȣ���ƽ�������ȷ����ƶ����������ƶ���������������ѹǿ����ƽ�������������֮�ͼ�С�ķ����ƶ������ϣ������¶Ȳ��䣬ƽ��״̬�ٺ͢ڵ�ƽ�ⳣ����ͬ��C���ƽ��ٱ�Ϊ�ڣ�ƽ��������Ӧ�����ƶ���SO2ת���ʱ��D�t4ʱ�̸ı�������ǿ����ǽ��»�ѹ�������£���ƽ�������ƶ���v����С�����ϣ�����ѹ����ƽ�������ƶ���v���������
���㣺���黯ѧ��Ӧ���ʺͻ�ѧƽ�⣬���鿼����ͼ��������������������

�����������������Դ������Ҫ�Ļ���ԭ�ϣ��ü�����������һ�����۵����ⷽ�����йص��Ȼ�ѧ����ʽ���£�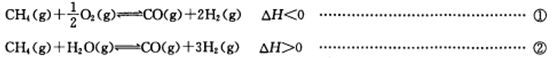
����˵������ȷ����
| A������Ӧ����v(CH4)��=v(CO)��ʱ�������÷�Ӧ��ƽ��״̬ |
| B��������������ʱ��������ϵѹǿ����Ӧ�١����м����ת���ʾ���С |
| C��ʹ�ø�Ч�������Լӿ췴Ӧ���ʣ�ͬʱ���CH4��ת���� |
| D��ͬһ������ͬʱ������Ӧ�����ʱ���������¶ȿ��ܱ��ֲ��� |
����������ȷ����
| A��pH��5��CH3COOH��Һ��pH��5��NH4Cl��Һ�У�ˮ�ĵ���̶���ͬ |
B��2SO2(g) + O2(g) 2SO3(g)�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯������ͼ��ʾ 2SO3(g)�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯������ͼ��ʾ |
C��2NO��2CO 2CO2��N2�Ħ�H��0�������¸÷�Ӧһ�����Է����� 2CO2��N2�Ħ�H��0�������¸÷�Ӧһ�����Է����� |
| D��25��Cʱ����Mg(OH)2������Һ�м���������NH4Cl���壬c(Mg2+)��С |
�ϳɰ��������������ú��ˮ��ԭ�Ͼ��ಽ��Ӧ�Ƶã����е�һ����ӦΪ��
CO��g��+ H2O(g) CO2(g) + H2(g) ��H ��0
CO2(g) + H2(g) ��H ��0
��Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ����д�ʩ����ȷ����
| A������ѹǿ | B�������¶� | C������CO ��Ũ�� | D���������� |
һ���¶��£���4���ݻ���Ϊ1 L�ĺ��������зֱ���з�Ӧ(��������A������)
A(s)+B(g)  C(g)+D(g) ��H ="+100" kJ��mol��1��ijʱ�̲�ò����������±���
C(g)+D(g) ��H ="+100" kJ��mol��1��ijʱ�̲�ò����������±���
| ������� | n(B)/mol | n(C)/mol | n(D)/mol | ��Ӧʱ��/min | ��Ӧ���� |
| �� | 0.06 | 0.60 | 0.10 | t1 | v(��)=v(��) |
| �� | 0.12 | 1.20 | 0.20 | t2 | |
| �� | 0.32 | 1.0 | 0 | 0 | |
| �� | 0.12 | 0.30 | | | v(��)=v(��) |
����˵����ȷ���� ( )
A����������ƽ����Ӧ����v(B)=0.04/t1 mol��L��1��min��1
B��t2ʱ��������v(��)��v(��)
C���������з�Ӧ��ƽ��ʱ����20 kJ
D����������c(D)=" 0.4" mol��L��1
���ڷ�ӦN2(g)+3H2(g) 2NH3(g) ��H=��92kJ/mol����ֻ�ı�����һ��������һ������������Ӧ������ʹƽ��������Ӧ�����ƶ����ǣ� ��
2NH3(g) ��H=��92kJ/mol����ֻ�ı�����һ��������һ������������Ӧ������ʹƽ��������Ӧ�����ƶ����ǣ� ��
| A�������¶� | B������������� |
| C������c(NH3) | D������������Ũ�Ⱦ�����ԭ����2�� |
��ҵ���Ʊ��ϳ����Ĺ�����Ҫ��ˮ�����������飺CH4(g) +H2O(g)��CO(g) +3H2(g) ��H��0����һ�������£������Ϊ1L���ܱ������г���1 mol CH4(g)��1mol H2O(g)�����H2O(g)��H2(g)��Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ����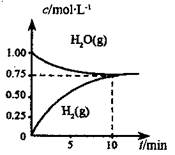
| A����ƽ��ʱ,CH4( g)��ת����Ϊ75% |
| B��0��10 min �ڣ�v(CO)��0.075 mol?L��1��min-1 |
| C���÷�Ӧ�Ļ�ѧƽ�ⳣ��K��0.1875 mol?L��1 |
| D����CH4(g)������������H2O(g)������������ȣ���Ӧ����ƽ�� |
 2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ����±�����ͼ��ʾ��
2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ����±�����ͼ��ʾ��
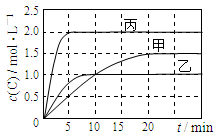
 2SO2(g)+O2(g)���������������������ʵ�����ʱ�䣨t)�仯��ʾ��ͼΪ
2SO2(g)+O2(g)���������������������ʵ�����ʱ�䣨t)�仯��ʾ��ͼΪ