题目内容
升高温度,下列数据不一定增大的是( )
| A.化学反应速率v | B.化学平衡常数K |
| C.水的离子积常数Kw | D.弱酸的电离常数Ka |
B
解析试题分析:A、升高温度,反应速率加快,故A不符合;
B、若正反应为放热反应,升高温度平衡向逆反应移动,化学平衡常数减小,若正反应为吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故B符合;
C、水的电离过程是吸热的,升高温度促进水的电离,升高温度电离程度增大,水的离子积增大,故C不符合;
D、弱电解质的电离是吸热过程,升高温度促进弱电解质的电离,电离平衡常数增大,故D不符合;
故选B.
考点:化学平衡常数的含义;离子积常数

练习册系列答案
相关题目
一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应如下:2A(g)+B(s) 2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
| | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 800 | 800 | 850 |
| c(A)起始/mol·L-1 | 1 | 2 | 1 |
| c(A)平衡/mol·L-1 | .0.5 | 1 | 0.85 |
| 放出的热量/kJ | a | b | c |
A.实验III的化学平衡常数K<1
B.实验放出的热量关系为b>2a
C.实验III在30min达到平衡时的速率v(A)为0.005mol? L-1·min-1
D.当容器内气体密度不随时间而变化时上述反应达到平衡
COCl2(g) CO(g)+Cl2(g); △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g); △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
一定条件下,在2L密闭容器中加入某A气体8.0mol,在4s时测得A气体的物质的量为5.6mol,则此4s内用A表示该反应速率正确的是: ( )
| A.0.3 mol·L-1s-1 | B.0.6 mol·L-1s-1 |
| C.1.0 mol·L-1s-1 | D.0.7 mol·L-1s-1 |
在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g) CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如下图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如下图所示,下列说法正确的是
A.平衡常数K= |
| B.该反应在T1时的平衡常数比T2时的小 |
| C.任意时刻,T2温度下的反应速率均大于T1温度下的速率 |
D.处于A点的反应体系从T1变到T2,达到平衡时 增大 增大 |
T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变化如图(Ⅰ)所示。保持其它条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示,下列结论正确的是( )
| A.图(Ⅱ)中T1>T2,则正反应是吸热反应 |
| B.t2 min时,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.其它条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大 |
| D.T℃时,若密闭容器中各物质起始浓度为:0.4 mol·L-1X、0.4 mol·L-1 Y、0.2mol/LZ保持其他 |
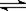 2SO3并达到平衡。在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡。在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是 xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。下列说法与图像符合的是
xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。下列说法与图像符合的是