在下列平衡2CrO42-(黄色)+ 2H+ Cr2O72-(橙红色)+ H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入
Cr2O72-(橙红色)+ H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入
| A.H+ | B.OH- | C.K+ | D.H2O |
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g)这是可逆反应,已知X2,Y2,Z的起始浓度分别为0.1摩尔/升,0.3摩尔/升,0.2摩尔/升,在一定条件下当反应达到平衡时,各物质浓度有可能是
2Z(g)这是可逆反应,已知X2,Y2,Z的起始浓度分别为0.1摩尔/升,0.3摩尔/升,0.2摩尔/升,在一定条件下当反应达到平衡时,各物质浓度有可能是
| A.Z为0.3摩尔/升 | B.Y2为0.4摩尔/升 |
| C.X2为0.2mol/L | D.Z为0.4摩尔/升 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列说法正确的是 
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始到10s时,Y的转化率为79.0% |
D.反应的化学方程式为: X(g)+Y(g) Z(g) Z(g) |
在2升的密闭容器中,反应物的物质的量为3mol,经过20s后,它的物质的量变成了1mol,在这20s内它的反应速率为 ( )
| A.0.1 mol / (L·S) | B.0.05mol /( L·min) |
| C.0.05mol / (L·S) | D.0.8mol / (L·S) |
下列事实不能用勒夏特列原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.红棕色的NO2加压后颜色先变深再变浅 |
| D.工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率 |
对于反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A.K=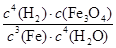 |
B.K=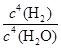 |
| C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小 |
| D.改变反应的温度,平衡常数不一定变化 |
一定质量的混合气体在密闭容器中发生如下反应:xA(g)+yB(g) zC(g)。达到平衡后,测得A气体的浓度为0.5mol/L。当恒温下将密闭容器的容积扩大到原来的二倍,再达平衡后,测得A的浓度为0.3mol/L。下列叙述正确的是
zC(g)。达到平衡后,测得A气体的浓度为0.5mol/L。当恒温下将密闭容器的容积扩大到原来的二倍,再达平衡后,测得A的浓度为0.3mol/L。下列叙述正确的是
| A.平衡向正反应方向移动 | B.x+y<z |
| C.C的体积分数降低 | D.B的转化率增大 |
已建立化学平衡的某可逆反应X(g)+2Y(g)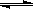 2Z(g),当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
2Z(g),当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
①生成物的质量分数一定增加,②生成物总量一定增加, ③反应物的转化率一定增大,
④反应物的浓度一定降低,⑤正反应速率一定大于逆反应速率,⑥一定使用催化剂
| A.①②③ | B.③④⑤ | C.②⑤ | D.④⑥ |
将等物质的量的F2和ClF混合,在密闭容器中发生反应:F2(g)+ClF(g) 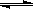 ClF3(g) ΔH<0。下列叙述正确的是
ClF3(g) ΔH<0。下列叙述正确的是
| A.保持恒容,平衡后再降低温度,平衡常数减小 |
| B.若增加F2的用量,平衡正向移动,则反应物的转化率均增大 |
| C.达到平衡后,若增大容器体积,则正反应速率减小,逆反应速率增大,平衡左移 |
| D.恒温恒容时,当ClF转化40%时,容器内的压强为初始时的0.8 |