题目内容
在2 L密闭容器中发生反应4A(s)+3B(g)=2C(g)+D(g),经2 min,B的物质的量减少0.6 mol,下列对该反应速率表示正确的是
A.在2 min末的反应速率:v (B)=0.3 mol·L-1·min-1
B.用A表示的反应速率为:v (A)=0.4 mol·L-1·min-1
C.用D表示的平均反应速率为:v (D)= 0.05 mol·L-1·min-1
D.分别用B、C表示的反应速率其比值为2∶3
C
解析试题分析:A、2min,B的物质的量减少0.6mol,则减少的B的物质的量浓度=0.6mol÷2L=0.3mol/L,所以用B物质表示的反应速率v(B)=0.3mol/L÷2min=0.15mol?L-1?min-1,A不正确;B、由于A物质为纯固体,则不能利用纯固体表示反应速率,故B错误;C、因为反应速率之比等于化学计量数之比,所以根据反应方程式可知用D表示的平均反应速率为v(D)=0.15mol?L-1?min-1×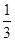 =0.05 mol?L-1?min-1,故C正确;D.反应速率之比等于化学计量数之比,则分别用B、C表示的反应速率其比值为3:2,所以D错误,答案选C。
=0.05 mol?L-1?min-1,故C正确;D.反应速率之比等于化学计量数之比,则分别用B、C表示的反应速率其比值为3:2,所以D错误,答案选C。
考点:考查反应速率的计算

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案在一定温度下,可逆反应:A2(气)+B2(气) 2AB(气),达到平衡的标志是
2AB(气),达到平衡的标志是
| A.容器的总压强不随时间而变化 |
| B.单位时间内有n molA2生成的同时有n molB2生成 |
| C.单位时间内有n molB2发生反应的同时有n molAB分解 |
| D.单位时间内生成n molA2同时就有2n molAB生成 |
下列说法正确的是
| A.放热反应在常温下一定很容易发生 |
| B.决定化学反应速率的主要因素是反应物的浓度、压强、温度、催化剂等 |
| C.熵增加且放热的反应一定是自发反应 |
| D.非自发的反应即不可能进行的反应 |
已建立化学平衡的某可逆反应X(g)+2Y(g) 2Z(g),当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
2Z(g),当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
①生成物的质量分数一定增加,②生成物总量一定增加, ③反应物的转化率一定增大,
④反应物的浓度一定降低,⑤正反应速率一定大于逆反应速率,⑥一定使用催化剂
| A.①②③ | B.③④⑤ | C.②⑤ | D.④⑥ |
判断反应过程自发性的目的
| A.判断反应的方向 | B.确定反应是否一定发生 |
| C.判断反应过程发生的速率 | D.判断反应过程的热效应 |
下列说法正确的是
| A.增大体系压强,活化分子数增加,化学反应速率一定增大 |
| B.加入反应物,使活化分子百分数增加,化学反应速率增大 |
| C.活化分子间所发生的分子间的碰撞均为有效碰撞 |
| D.升高温度,活化分子百分数增加,化学反应速率一定增大 |
化学平衡常数(K)是化学反应限度的一个重要参数,该常数表示的意义是可逆反应进行的程度,K值越大,表示的意义错误的是( )
| A.温度越高 | B.反应物浓度越小 |
| C.反应进行的越完全 | D.生成物浓度越大 |
已知反应:2SO2(g)+O2(g)  2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是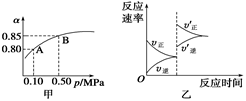
| A.由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
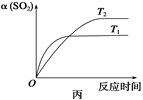
| D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
 2B(g)+C (g),下列能说明反应已达平衡状态的是
2B(g)+C (g),下列能说明反应已达平衡状态的是