在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)  ?nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
?nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
| 容器体积/L 温度/℃ c(Y)/mol·L-1 | 1 L | 2 L | 4 L |
| 100℃ | 1.00 | 0.75 | 0.53 |
| 200℃ | 1.20 | 0.90 | 0.63 |
| 300℃ | 1.30 | 1.00 | 0.70 |
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
密闭容器中一定量的混合气体发生反应:xA(g)+yB(g)  zC(g),平衡时,测得A的浓度为0.50 mol/L,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30 mol/L,有关叙述不正确的是( )
zC(g),平衡时,测得A的浓度为0.50 mol/L,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30 mol/L,有关叙述不正确的是( )
| A.平衡一定向右移动 | B.B的转化率降低 |
| C.x+y>z | D.C的体积分数降低 |
关节炎病因是在关节滑液中形成尿酸钠晶体,尤其在寒冷季节易诱发关节疼痛其化学机理为:
① HUr + H2O  Ur- + H3O+ ②Ur- (aq)+Na+(aq)
Ur- + H3O+ ②Ur- (aq)+Na+(aq)  NaUr(s)
NaUr(s)
(尿酸) (尿酸根离子)
下列对反应②叙述中正确的是( )
| A.反应的△H>0 | B.反应的△H<0 |
| C.升高温度平衡向正反应方向移动 | D.改变温度不影响平衡移动 |
乙酸蒸气能形成二聚分子2CH3COOH(g)  (CH3COOH)2 (g) Δ H<0 ,欲测定单体乙酸的相对分子质量,应采用的条件是( )
(CH3COOH)2 (g) Δ H<0 ,欲测定单体乙酸的相对分子质量,应采用的条件是( )
| A.高温低压 | B.低温高压 | C.低温低压 | D.高温高压 |
在一定条件下,对于反应mA(g)+nB(g) cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的ΔH和ΔS判断正确的是( )
cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的ΔH和ΔS判断正确的是( )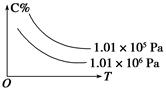
| A.ΔH<0 ΔS>0 | B.ΔH>0 ΔS<0 |
| C.ΔH>0 ΔS>0 | D.ΔH<0 ΔS<0 |
在水溶液中,重铬酸钾K2Cr2O7存在以下平衡: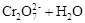

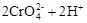 ,下列说法正确的是
,下列说法正确的是
| A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 |
| B.该反应不是氧化还原反应 |
| C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
D.该反应的平衡常数表达式是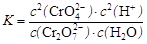 |
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s) ΔH>0
Z(g)+W(s) ΔH>0
下列叙述正确的是
| A.加入少量W,逆反应速率增大 | B.当容器中气体的密度不变时,反应达到平衡 |
| C.升高温度,Y的百分含量增加 | D.平衡后加入X,上述反应的ΔH增大 |
下列有关化学反应速率的说法中,正确的是
| A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B.用铁片和稀硫酸反应制取氢气,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C.在做草酸与高锰酸钾的反应时,加入少量硫酸锰固体可加快溶液褪色速率 |
| D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,为了加快反应速率,实际生活中使用了增大压强或升高温度的方法。 |
据报道,在300 ℃、70 MPa下由二氧化碳和氢气合成乙醇已成为现实
2CO2(g) + 6H2(g) CH3CH2OH(g) + 3H2O(g)下列叙述错误的是
CH3CH2OH(g) + 3H2O(g)下列叙述错误的是
| A.使用催化剂可大大提高生产效率 |
| B.反应需在300 ℃进行可推测该反应是吸热反应 |
| C.充入大量CO2气体可提高H2的转化率 |
| D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率 |