判断一个化学反应的自发性常用焓判据和熵判据,则在下列情况下,可以判定反应一定自发进行的是
| A.ΔH>0,ΔS>0 | B.ΔH<0,ΔS>0 | C.ΔH>0,ΔS<0 | D.ΔH<0,ΔS<0 |
以下各条件的改变可确认发生了化学平衡移动的是 ( )
| A.化学反应速率发生了改变 |
| B.有气态物质参加的可逆反应达到平衡后,改变了压强 |
| C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
| D.可逆反应达到平衡后,加入了催化剂 |
改变下列条件,能使N2(g)+3H2(g) 2NH3(g) △H<0平衡向逆反应方向移动的是
2NH3(g) △H<0平衡向逆反应方向移动的是
| A.升高温度 | B.增大压强 | C.增大H2的浓度 | D.使用催化剂 |
在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发 生反应:H2(g)+Br2(g)  2HBr(g) ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g) ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
| A.由图可知:T2>T1 |
| B.a、b两点的反应速率:b>a |
| C.为了提高Br2(g)的转化率,可采取增加Br2(g)通入量的方法 |
| D.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
有一容积固定的密闭反应器,中间有一个可自由移动的导热的隔板将容器分成甲、乙两部分,分别发生下列两个可逆反应:
甲:a(g)+b(g)  2c(g) ΔH1<0、 乙: x(g)+3y(g)
2c(g) ΔH1<0、 乙: x(g)+3y(g)  2z(g) ΔH2>0
2z(g) ΔH2>0
起初甲、乙均达到反应平衡后隔板位于正中间,然后进行相关操作后,下列叙述错误的是( )
| A.绝热下向甲中通入惰性气体,c的物质的量不变 |
| B.绝热下向乙中通入z气体,反应器中温度升高 |
| C.恒温下向甲中通入惰性气体,甲中平衡不移动,乙中X、Y的转化率增大 |
| D.恒温下向乙中通入z气体,y的物质的量浓度增大 |
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 2CO2(g)+S(l) ΔH<0若反应在恒容的密闭容器中进行,下列有关说法正确的是 ( )
2CO2(g)+S(l) ΔH<0若反应在恒容的密闭容器中进行,下列有关说法正确的是 ( )
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
2NH3(g)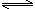 N2(g)+3H2(g) △H=+92.4kJ/mol
N2(g)+3H2(g) △H=+92.4kJ/mol
实验测的起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| NH3 | N2 | H2 | ||
| ① | 2 | 0 | 0 | 吸收热量akJ |
| ② | 0 | 1 | 3 | 放出热量bkJ |
| ③ | 4 | 0 | 0 | 吸收热量ckJ |
下列叙述正确的是
A.热量关系:a=b
B.反应的平衡常数:③>①>②
C.达平衡时H2的体积分数:①>③
D.①中的密度不再改变时说明反应已达到平衡状态
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H="74.9" kJ·mol-1,下列说法中正确的是
| A.该反应中熵变、焓变皆大于0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
在体积恒定的密闭容器中,一定量的SO2与1mol O2在催化剂作用下加热到600℃发生反应:
2SO2+O2 2SO3 △H<0。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述正确的是
2SO3 △H<0。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述正确的是
| A.当SO3的生成速率与SO2的消耗速率相等时反应达到平衡 |
| B.降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| C.将平衡混合气体通入过量BaCl2溶液中,会得到两种白色沉淀 |
| D.该反应过程中转移了2mol电子 |
 pC(g)+qD(g) △H<0。下列结论中错误的是
pC(g)+qD(g) △H<0。下列结论中错误的是