题目内容
在体积恒定的密闭容器中,一定量的SO2与1mol O2在催化剂作用下加热到600℃发生反应:
2SO2+O2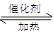 2SO3 △H<0。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述正确的是
2SO3 △H<0。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述正确的是
| A.当SO3的生成速率与SO2的消耗速率相等时反应达到平衡 |
| B.降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| C.将平衡混合气体通入过量BaCl2溶液中,会得到两种白色沉淀 |
| D.该反应过程中转移了2mol电子 |
D
解析试题分析:结合方程式,当气体的物质的量减少0.5mol时消耗氧气0.5mol,转移的电子数为2mol,达平衡时将混合气体通入BaCl2溶液中,会生成BaSO4,降低温度时,正反应速率减小程度小于逆反应速率的减小程度,A项SO3的生成速率与SO2的消耗速率的方向相同,不能确定是否平衡。
考点:化学平衡的标志、温度对反应速率的影响、电子转移。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关说法正确的是 ( )
| A.合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动 |
| B.常温下,将pH =10的氨水稀释,溶液中所有离子浓度都减小 |
| C.100 mL pH=3的HA和HB分别与足量的锌反应,HA放出的氢气多,说明HA酸性比HB弱 |
D.已知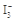  I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
在一固定容积的密闭容器中,可逆反应: H2(g) + I2(g) 2HI (g)达到平衡的标志是
2HI (g)达到平衡的标志是
| A.H2、I2、HI的分子数之比为1∶1∶2 |
| B.混合气体的颜色不再发生变化 |
| C.单位时间生成n mol H2,同时消耗成2n mol HI |
| D.混合气体的密度保持不变 |
下列事实中,能用勒沙特列原理来解释的是
| A.由H2(g)、I2(g)、HI(g)组成的混合气体平衡体系加压后颜色加深 |
| B.久置的氯水变成了稀盐酸 |
| C.在FeCl3溶液中加入铁粉防止氧化变质 |
| D.加入催化剂有利于SO2与O2反应制SO3 |
在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发 生反应:H2(g)+Br2(g)  2HBr(g) ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g) ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
| A.由图可知:T2>T1 |
| B.a、b两点的反应速率:b>a |
| C.为了提高Br2(g)的转化率,可采取增加Br2(g)通入量的方法 |
| D.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
现有下列两个图象: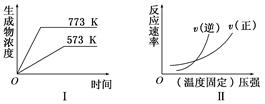
下列反应中符合上述图象的是( )
A.N2(g) + 3H2(g) 2NH3(g) ΔH<0 2NH3(g) ΔH<0 |
B.2SO3(g) 2SO2(g) + O2(g) ΔH>0 2SO2(g) + O2(g) ΔH>0 |
C.4NH3(g) + 5O2(g) 4NO(g) + 6H2O(g) ΔH<0 4NO(g) + 6H2O(g) ΔH<0 |
D.H2(g) + CO2(g)  CO(g) + H2O(g) ΔH>0 CO(g) + H2O(g) ΔH>0 |
一定温度下,将1molA和1molB气体充入2L恒容密闭容器,发生反应A(g)+ B(g) xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是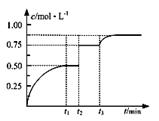
| A.反应方程式中的x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量物质D |
| D.t1~t3间该反应的平衡常数均为4 |
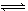 2C来说,以下表示的化学反应速率最快的是
2C来说,以下表示的化学反应速率最快的是 2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的
2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的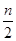 )
)