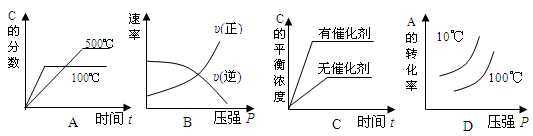
在密闭容器中进行如下反应:H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是
| A.T1>T2,△H>0 | B.T1> T2,△H<0 |
| C.T1<T2,△H>0 | D.T1< T2,△H<0 |
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)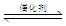 2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
下列有关平衡常数说法正确的是
| A.温度越高,K值越大 |
| B.K值越大,反应的转化率越小 |
| C.K值越大,反应的转化率越大 |
| D.K值的大小与起始浓度有关 |
在四个不同的容器中,分别进行不同条件下的合成氨反应N2(g)+3H2(g) 2NH3(g)。在相同时间内表示该反应速率最快的是
2NH3(g)。在相同时间内表示该反应速率最快的是
| A.v(H2)=0.1 mol/(L·s) | B.v(N2)=0.1 mol/(L·s) |
| C.v(N2)=0.2 mol/(L·s) | D.v(NH3)=0.3 mol/(L·s) |
难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下: TaS2(g)+ 2I2(g)TaI4(g) + S2(g),下列说法错误的是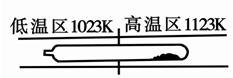
| A.在不同温度区域,TaI4 的量不同 |
| B.在提纯过程中,S2 的量不断增多 |
| C.该反应的平衡常数不随TaI4 和S2 的浓度增大而增大 |
| D.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区 |
在恒容密闭容器进行的可逆反应:MgSO4(s) + CO(g)  MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
| A.若平衡常数K值变大,平衡移动时v逆先减小后增大 |
| B.容器中固体物质的质量不再改变,则反应到达平衡状态 |
| C.若x表示温度,y可表示平衡时混合气体的密度 |
| D.若x表示CO物质的量,y可表示平衡时CO2与CO物质的量之比 |
下列事实不能用平衡移动原理解释的是
 |      |  |  |
| A | B | C | D |
CO(g)+H2O(g) CO2(g)+H2(g)+Q,将1molCO和1molH2O置于密闭容器中发生上述反应,其他条件不变的情况下,下列叙述正确的是
CO2(g)+H2(g)+Q,将1molCO和1molH2O置于密闭容器中发生上述反应,其他条件不变的情况下,下列叙述正确的是
| A.加入催化剂,改变了反应的途径,反应放出的热量也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.若将该反应设计成原电池,反应放出的热量不变 |
800℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应
CO(g)+H2O(g) CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
下列说法正确的是
A.反应在t1min内的平均速率为v(H2)=
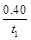 mol/(L·min)
mol/(L·min)B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2O,到达平衡时n(CO2)=0.40 mol
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D.温度升至1000℃,上述反应平衡常数为1.6,则正反应为放热反应
 2C(g) △H<0,下列各图中正确的是
2C(g) △H<0,下列各图中正确的是