一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g)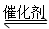 2CO2(g)+S(l) ΔH<0
2CO2(g)+S(l) ΔH<0
若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
处于平衡状态的反应2 H2 S(g)  2H2(g)+S2(g)
2H2(g)+S2(g)  H>0,不改变其他条件的情况下合理的说法是
H>0,不改变其他条件的情况下合理的说法是
A.加入催化剂,反应途径将发生改变, H也将随之改变 H也将随之改变 |
| B.升高温度,正逆反应速率都增大,H2S分解率也增大 |
| C.增大压强,平衡向逆反应方向移动,将引起体系温度降低 |
| D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小 |
下列表格中的各种情况,可以用下面的图象曲线表示的是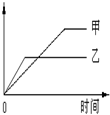
| | 反应 | 纵坐标 | 甲 | 乙 |
| A | 等质量钾、钠分别与足量水反应 | H 2质量 | 钠 | 钾 |
| B | 相同质量氨气,在同一容器中 2NH3 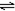 N2+3H2 ΔH >0 N2+3H2 ΔH >0 | 氨气的转化率 | 500℃ | 400℃ |
| C | 在体积可变的恒压容器中,体积比1:3的N2、H2,N2+3H2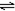 2NH3 2NH3 | 氨气的浓度 | 活性一般的催化剂 | 活性高的催化剂 |
| D | 2molSO2与lmolO2,在相同温度下2SO2(g)+O2(g)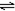 2SO3(g) 2SO3(g) | SO3物质的量 | 2个大气压 | 10个大气压 |
一定温度下,在2L的密闭容器中,X、 Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
下列描述正确的是
| A.反应开始到10s,用Z表示的反应速率为0.158 mol/(L·s)-1 |
| B.反应开始到l0s,X的物质的量浓度减少了0.79 mol/L |
| C.反应开始到10S时,Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |
向绝热恒容密闭容器中通入SO2和NO2,发生反应SO2(g)+NO2(g)=SO3(g)+NO(g),其正反应速率(v)随时间(t)变化的关系如下图所示。下列结论中错误的是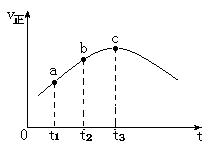
| A.反应在c点达到平衡状态 |
| B.反应物的浓度:a点大于b点 |
| C.反应物的总能量高于生成物的总能量 |
| D.逆反应速率:c点大于b点 |
T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图甲所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图乙所示。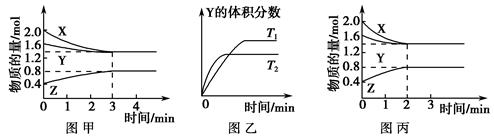
则下列结论正确的是(双选) ( )。
A.该反应可表示为3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.若其他条件不变,升高温度,平衡将向逆反应方向移动 |
| C.若其他条件不变,开始时将该容器压缩为1 L,则反应将按图丙进行 |
| D.若其他条件不变,使用适当的催化剂,则反应可以按图丙进行 |
为了变废为宝,控制温室效应,工业上可用CO2来生产甲醇。一定条件下发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。
CH3OH(g)+H2O(g)。如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。
| A.降低温度 |
| B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离出来 |
| D.再充入1 mol CO2和3 mol H2 |
在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3—(aq)。测得不同温度下该反应的平衡常数K如表所示:
I3—(aq)。测得不同温度下该反应的平衡常数K如表所示:
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1 100 | 841 | 689 | 533 | 409 |
下列说法正确的是( )。
A.反应I2(aq)+I-(aq)
 I3—(aq)的ΔH>0
I3—(aq)的ΔH>0B.其他条件不变,升高温度,溶液中c(I3—)减小
C.该反应的平衡常数表达式为K=
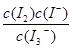
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是( )。
2Z(g)一定达到化学平衡状态的是( )。
①X、Y、Z的物质的量之比为1∶2∶2 ②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |
化学平衡常数可以用K来表示,下列关于化学平衡常数的说法中正确的是( )。
| A.K越大,反应物的转化率越小 |
| B.K与反应物的浓度有关 |
| C.K与生成物的浓度有关 |
| D.K与温度有关 |