在2L恒容密闭容器中充入2 mol X和lmol Y发生反应:2X(g)+Y(g) 3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
| A.升高温度,平衡常数增大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.Q点时,Y的转化率最大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol·L—1的NaOH溶液。整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是
| A.实验进程中可用pH试纸测定溶液的pH |
B.c点所示溶液中: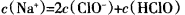 |
| C.向a点所示溶液中通入SO2,溶液的酸性和漂白性均增强 |
D.由a点到b点的过程中,溶液中 减小 减小 |
下列各示意图与对应的表述正确的是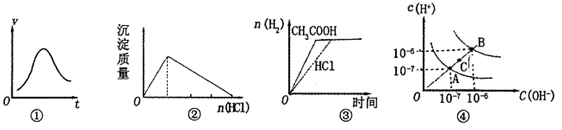
| A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 |
| B.图②表示在四羟基合铝酸钠溶液中加入盐酸,产生沉淀的质量变化 |
| C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化 |
| D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
在1L密闭容器发生反应:4NH3(g)+5O2(g) 4NO(g)+6HO(g) △H=-Q kJ· mol-1(Q>0),容器内部分物质的物质的量浓度如下表:
4NO(g)+6HO(g) △H=-Q kJ· mol-1(Q>0),容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)( mol·L-1) | c(O2)( mol·L-1) | c(NO)( mol·L-1) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
| 第10min | 0.7 | 1.475 | 0.1 |
A.反应在第2min到第4min时,O2的平均速率为0.1875 mol·L-1·min-1
B.反应在第2min时改变了某一条件,该条件可能是使用催化剂或升高温度
C.第4min、第8min时分别达到化学平衡,且平衡常数相同
D.在开始反应的前2min内,该反应放出0.05QKJ的热量
在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)  2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是
2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是
| A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 |
| B.15℃时氨基甲酸铵的分解平衡常数为2.048×10-9(mol/L)3 |
| C.恒温下压缩体积,NH3的体积分数减小 |
| D.再加入一定量氨基甲酸铵,可加快反应速率 |
mA(g)+nB(g) 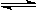 pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
| A.③④⑤⑥ | B.②③④⑥ | C.①③④⑤ | D.①③④⑥ |
一定温度下,对于反应N2+O2 2NO在密闭容器中进行,下列措施能增大反应速率的是 ( )。
2NO在密闭容器中进行,下列措施能增大反应速率的是 ( )。
| A.降低温度 | B.恒容充入氮气 | C.恒压充入氦气 | D.恒容充入氦气 |
如图是关于反应A2(g)+3B2(g) 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )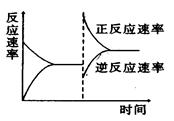
| A.升高温度,同时加压 | B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 | D.增大反应物浓度,同时使用催化剂 |
在密闭容器中进行如下反应:X2(g)+Y2(g)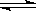 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A.Z为0.3mol/L | B.Y2为0.4mol/L | C.X2为0.2mol/L | D.Z为0.4mol/L |
 2C,达到化学反应限度时,B的物质的量可能是( )
2C,达到化学反应限度时,B的物质的量可能是( )