在一定温度下,将气体X和气体Y各0.16mol充入10 L恒容密闭容器中,发生反应:
X(g)+Y(g) 2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2 min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C.保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol 气体Y,到达平衡时,n(Z)<0.24 mol
D.其他条件不变,向平衡体系中再充入0.16mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大
下列实验过程中曲线变化不正确的是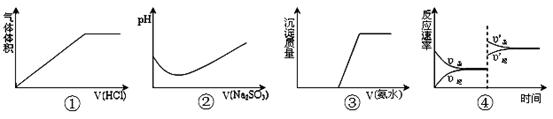
| A.①表示Na2CO3溶液中滴入稀盐酸 |
| B.②表示溴水中滴入Na2SO3溶液 |
| C.③表示HCl和MgCl2溶液中滴入氨水 |
D.④表示一定条件下反应:2SO2+O2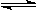 2SO3 ΔH< 0 ,达平衡后,增大压强 2SO3 ΔH< 0 ,达平衡后,增大压强 |
化学平衡状态I、II、III的相关数据如下表:
| 编号 | 化学方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| I | Fe(s)+CO2(g) 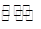 2 FeO(s)+CO(g) 2 FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| II | CO(g)+H2O(g) 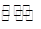 CO2(g)+H2(g) CO2(g)+H2(g) | K2 | 1.62 | b |
| III | Fe(s)+H2O(g)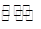 FeO(s)+H2(g) FeO(s)+H2(g) | K3 | a | 1.68 |
A.a>b B.增大压强,平衡状态II不移动
C.升高温度平衡状态III向正反应方向移动 D.反应II、III均为放热反应
在一定条件下,将E(g)和F(g)充入体积不变的2 L密闭容器中,发生下述反应,并于5 min末达到平衡:2E(g)+F(g) 2G(g)。有关数据如下:
2G(g)。有关数据如下:
| | E(g) | F(g) | G(g) |
| 初始浓度(mol?L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol?L-1) | c1 | c2 | 0.4 |
A.反应在前5min内,v(E)=0.04 mol/(L·min)
B.其他条件不变,若增大E的浓度,则达平衡时E的转化率会增大
C.其他条件不变,降低温度,平衡时n(E)=3.0mol,则反应的△H>0
D.平衡后移走2.0 mol E和1.0 mol F,在相同条件下再达平衡时,c(G)<0.2 mol?L-1
下列说法正确的是( )
| A.增大压强,活化分子数增加,化学反应速率一定增大 |
| B.升高温度,活化分子百分数增加,化学反应速率一定增大 |
| C.活化分子间所发生的分子间的碰撞为有效碰撞 |
| D.增大反应物浓度,使活化分子百分数增加,化学反应速率增大 |
下列措施对增大反应速率明显有效的是( )
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.在H2SO4与Na2CO3两溶液反应时,增大压强 |
D.反应N2+3H2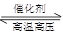 2NH3恒容增加氮气 2NH3恒容增加氮气 |
一定条件下,向密闭恒容容器中加入1.0 mol·L-1X,发生反应:2X(g)  Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是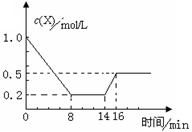
| A.0~8min用Y表示该反应速率为0.1mol·L-1·min-1 |
| B.8min时达到平衡,该反应的平衡常数为K= 0.5 |
| C.14min时,改变的反应条是降低了温度 |
| D.16min时的正反应速率比8min时的正反应速率大 |
可逆反应2NO2 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n mol NO2
②用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
| A.①③⑤ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
少量铁片与l00 mL 0.01 mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加KNO3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10 mL 0.1 mol/L盐酸
| A.①⑥⑦ | B.③⑤⑧ | C.③⑦⑧ | D.③④⑥⑦⑧ |
 B+C(g) ΔH=" +Q" kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
B+C(g) ΔH=" +Q" kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是