题目内容
在一定温度下,将气体X和气体Y各0.16mol充入10 L恒容密闭容器中,发生反应:
X(g)+Y(g) 2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2 min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C.保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol 气体Y,到达平衡时,n(Z)<0.24 mol
D.其他条件不变,向平衡体系中再充入0.16mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大
D
解析试题分析:A、2min内Y物质的量变化为0.16mol-0.12mol=0.04mol,故v(Y)=0.04mol÷10L÷2min=0.002mol/(L?min),速率之比等于化学计量数之比,故v(Z)=2v(Y)=2×0.002mol/(L?min)=0.004mol/(L?min),错误;B、该反应正反应是放热反应,降低温度平衡向正反应移动,反应达到新平衡前v(逆)<v(正),错误;C、保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol 气体Y,X、Y的比值相同,因为该反应前后气体的系数不变,所以两次平衡为等效平衡,到达平衡时,n(Z)="0.24" mol,错误;D、其他条件不变,向平衡体系中再充入0.16mol气体X,平衡向正反应方向移动,所以达到新平衡时,气体Y的转化率增大,X的体积分数增大,正确。
考点:本题考查反应速率的计算、化学平衡移动、等效平衡。

练习册系列答案
相关题目
一定温度下,在体积一定的密闭容器中进行的可逆反应:C(s) + CO2(g)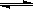 2CO(g),不能判断反应已经达到化学平衡状态的是
2CO(g),不能判断反应已经达到化学平衡状态的是
| A.v(CO2)= v(CO) | B.容器中总压强不变 |
| C.容器中混合气体的密度不变 | D.容器中CO的体积分数不变 |
把下列4种Na2S2O3溶液和相应体积的水,分别加入4个盛有20 mL 2 mol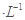 硫酸的烧杯中,此时,Na2S2O3和H2SO4缓慢地进行反应:
硫酸的烧杯中,此时,Na2S2O3和H2SO4缓慢地进行反应: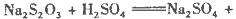
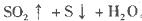 其中最早出现明显浑浊的是
其中最早出现明显浑浊的是
A.25 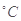 .20 mL 3 mol .20 mL 3 mol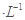 的Na2S2O3溶液,25 mL蒸馏水 的Na2S2O3溶液,25 mL蒸馏水 |
B.0 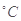 .30 mL 2 mol .30 mL 2 mol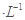 的Na2S2O3溶液,15 mL蒸馏水 的Na2S2O3溶液,15 mL蒸馏水 |
C.25 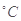 .10 mL 4 mol .10 mL 4 mol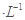 的Na2S2O3溶液,35 mL蒸馏水 的Na2S2O3溶液,35 mL蒸馏水 |
D.0 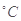 .10 mL 2mol .10 mL 2mol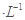 的Na2S2O3溶液,35 mL蒸馏水 的Na2S2O3溶液,35 mL蒸馏水 |
下列措施对增大反应速率明显有效的是( )
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.在H2SO4与Na2CO3两溶液反应时,增大压强 |
D.反应N2+3H2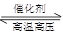 2NH3恒容增加氮气 2NH3恒容增加氮气 |
下列对“化学反应速率”的理解正确的是
| A.化学反应速率表示的是化学反应进行的限度 |
| B.化学反应速率可以用单位时间内反应物浓度的减少量来表示 |
| C.对于任何化学反应来说,反应速率越快,反应现象就越明显 |
| D.化学反应速率可以是正值,也可以是负值 |
在一不可变容器中发生如下反应:2NO2 2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
| A.密度 | B.颜色 | C.压强 | D.总物质的量 |
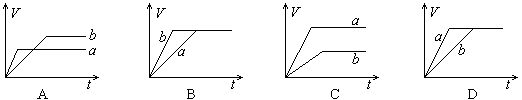
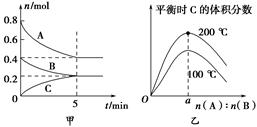
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是