可逆反应A(g)+ 4B(g) C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
| A.vA==0.15mol/(L·min) | B.vB="=0.6" mol/(L·min) |
| C.vC="=0.4" mol/(L·min) | D.vD="=0.01" mol/(L·s) |
在密闭容器中进行如下反应:I2(g)+H2(g)  2HI(g),已知I2、H2、HI的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
2HI(g),已知I2、H2、HI的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
| A.HI为0.4mol/L | B.H2为0.15mol/L | C.I2为0.2mol/L | D.HI为0.35mol/L |
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是( )
| A.减小压强能增大反应速率 | B.增大压强能减小反应速率 |
| C.使用适当的催化剂能增大反应速率 | D.升高温度对反应速率无影响 |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( ) 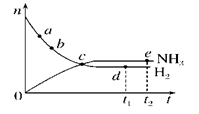
| A.c点处正反应速率和逆反应速率相等 |
| B.a点处正反应速率比b点处的大 |
| C.d点(t1时刻)和e点(t2时刻)处n(N2)不同 |
| D.t2时刻,正反应速率大于逆反应速率 |
为探究锌与稀盐酸反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断正确的是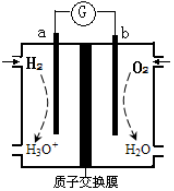
| A.加入铜粉,v(H2)增大 |
| B.加入NaHSO4固体,v(H2)不变 |
| C.加入水,锌不与水反应,v(H2)不变 |
| D.加入NaCl固体,会增大Cl-浓度,使v(H2)增大 |
对于300mL 1 mol·L-1盐酸与铁片的反应,采取下列措施:
①升高温度 ②改用100mL 3 mol·L-1盐酸
③再加300mL 1 mol·L-1盐酸 ④用等量铁粉代替铁片 ⑤改用100mL 98%的硫酸
其中能使反应速率加快的是
| A.①②④ | B.①③④ | C.①②③④ | D.①②③⑤ |
对于反应2SO2+O2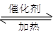 2SO3,下列判断正确的是
2SO3,下列判断正确的是
| A.2 mol SO2和足量的O2反应,一定生成2mol SO3 |
| B.平衡时SO2、O2、SO3的分子数之比为2∶1∶2 |
| C.平衡时SO2的消耗速率等于O2的生成速率的2倍 |
| D.平衡时SO2的浓度为O2浓度的2倍 |
 ?pC(g)+2D(g),生成0.5 mol D,又知C的平均反应速率是0.1 mol/(L·s),则下列说法中正确的是
?pC(g)+2D(g),生成0.5 mol D,又知C的平均反应速率是0.1 mol/(L·s),则下列说法中正确的是
 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是