题目内容
等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4,下列图中表示其产生H2总体积(V)与时间(t)的关系正确的是( ) 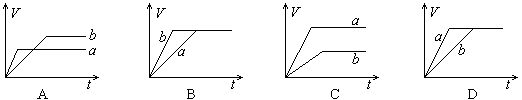
A
解析试题分析:Zn能够与酸发生置换反应产生氢气,由于酸过量,所以反应放出氢气的多少按照Zn来确定。由于在a中同时加入少量CuSO4,Zn会发生反应:Zn+ CuSO4=ZnSO4+Cu.Zn减少,放出氢气的量也减少,但是由于Zn、Cu及硫酸形成了原电池,加快了反应速率,所以a比b反应速率快,但是量比b少些,选项的A。
考点:考查原电池反应对方向反应速率的影响的知识。

练习册系列答案
相关题目
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如下图。下列叙述中正确的是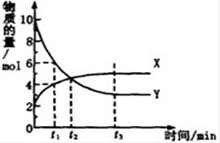
| A.反应的化学方程式为5Y?X |
| B.t1时,Y的浓度是X浓度的1.5倍 |
| C.t2时,正、逆反应速率相等 |
| D.t3时,逆反应速率大于正反应速率 |
一定温度下,将1molA(g)和1molB(g)充入2 L密闭容器中发生反应,在t1时达到平衡:A(g)+B(g) xC(g)+D(s)。在t2、t3时刻分别改变反应的一个条件(温度、体积、催化剂或一种物质),测得容器中C(g)的浓度随时间变化如图所示。有关说法正确的是
xC(g)+D(s)。在t2、t3时刻分别改变反应的一个条件(温度、体积、催化剂或一种物质),测得容器中C(g)的浓度随时间变化如图所示。有关说法正确的是
( ) 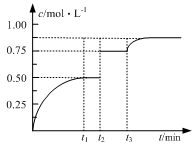
| A.反应方程式中x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量D |
| D.t1~t3间该反应的平衡常数均相同 |
下列措施是为了降低化学反应速率的是
| A.食品放在冰箱中贮藏 |
| B.双氧水制氧气时加入少量二氧化锰 |
| C.试管中进行镁和水反应时,稍微加热 |
| D.铁粉代替铁钉与稀硫酸反应制取氢气 |
在一定温度下,将气体X和气体Y各0.16mol充入10 L恒容密闭容器中,发生反应:
X(g)+Y(g) 2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2 min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C.保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol 气体Y,到达平衡时,n(Z)<0.24 mol
D.其他条件不变,向平衡体系中再充入0.16mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大
 2B(g)+C(g),若A的浓度由0.1 mol·L
2B(g)+C(g),若A的浓度由0.1 mol·L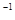 降到0.06 mol·L
降到0.06 mol·L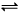 2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是  2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是