由金红石(TiO2)制取单质Ti涉及到的步骤为:
TiO2 TiCl4
TiCl4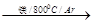 Ti
Ti
已知:①C(s)+O2(g)=CO2(g) DH=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) DH=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) DH=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH是
| A.-80kJ·mol-1 | B.-160kJ·mol-1 | C.160kJ·mol-1 | D.80kJ·mol-1 |
研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们视为一种潜在的清洁燃料。液氨燃烧的化学反应方程式为:4NH3+3O2 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
| 燃料 | 沸点(℃) | 燃烧热(kJ/mol) | 相对分子质量 | 液态密度(g/cm3) |
| 氢 | -252.6 | 238.40 | 2.02 | 0.07 |
| 氨 | -33.50 | 317.10 | 17.03 | 0.61 |
①以氨和氢为燃料时,可以减缓温室效应
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量多
④氨的液化比氢容易得多
A.①③ B.②③ C.①④ D.②④
灰锡(以粉末状态存在)和白锡是锡的两种同素异形体。已知:
① Sn(s、白) + 2HCl(aq) → SnCl2(aq) + H2(g) + Q1
② Sn(s、灰) + 2HCl(aq) → SnCl2(aq) + H2(g) + Q2
 ③ Sn(s、灰)
③ Sn(s、灰)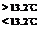 Sn(s、白) + Q3, Q3=" -" 2.1kJ
Sn(s、白) + Q3, Q3=" -" 2.1kJ
根据以上信息推断正确的是
| A.灰锡、白锡的互相转化是可逆反应 | B.常温下锡以灰锡状态存在 |
| C.反应中的能量变化:Q1 < Q2 | D.长期处于13.2℃以下,锡制器皿会自行毁坏 |
已知:S(s)+O2(g)→SO2(g) +297.16kJ,2SO2(g)+O2(g) 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是
| A.1 molSO2(g)的能量总和大于lmol S(s)和l molO2(g)的能量总和 |
| B.将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出196.6kJ的热量 |
C.S(g)+O2(g) SO2(g)+Q,Q值小于297.16 kJ SO2(g)+Q,Q值小于297.16 kJ |
| D.当l mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46kJ的热量 |
根据碘与氢气反应的热化学方程式
(i)I2(g)+ H2(g)  2HI(g)+ 9.48 kJ (ii) I2(s)+ H2(g)
2HI(g)+ 9.48 kJ (ii) I2(s)+ H2(g) 2HI(g) - 26.48 kJ
2HI(g) - 26.48 kJ
下列判断正确的是
| A.1mol I2(s)中通入2gH2(g),反应吸热26.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(ii)的反应物总能量比反应(i)的反应物总能量低 |
| D.反应(i)放出的热量多,所以产物的能量低,比反应(ii)的产物更稳定 |
下列燃烧反应的反应热不是燃烧热的是
①H2(g)+O2(g)=H2O(l) ΔH1 ②C(s)+O2(g)=CO(g) ΔH2
③S(s)+O2(g)=SO2(g) ΔH3 ④2H2S(g)+3O2(g)=2SO2(s)+2H2O(l) ΔH4
| A.①③ | B.②④ | C.②③ | D.①④ |
某废水处理厂处理废水中NH+的过程如下:
①NH4+(aq)+ O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH="-b" KJ/mol
O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH="-b" KJ/mol
②2HNO2(aq)+O2(g)=2NO3-(aq)+2H+ ΔH=-aKJ/mol
下列叙述正确的是( )
| A.将NH4+转化为NO3-的热化学方程式可表示为: NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(1)ΔH=-(b+  )KJ/mol )KJ/mol |
| B.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱 |
| C.常温下,若HNO3溶液中c(H+)="0.1" mol·L-1,则该溶液的pH>1 |
| D.若上述两次转化完全,不考虑其它杂质离子的存在,则:c(NH4+)+c(OH-)=c(NO3-)+c(H+) |
已知Zn(s)+ H2SO4(aq)= ZnSO4(aq)+ H2(g) ΔH<0;则下列叙述不正确的是
| A.该反应的ΔH值与反应物用量无关 |
| B.该反应的化学能可以转化为电能 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应中反应物的化学键断裂放出能量,生成物化学键形成吸收能量 |