在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l);ΔH="+725.8" kJ/mol O2(g)=CO2(g)+2H2O(l);ΔH="+725.8" kJ/mol |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);ΔH=-1452 kJ/mol |
| C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);ΔH=-725.8 kJ/mol |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);ΔH="+1452" kJ/mol |
下列关于化学反应与能量的说法正确的是
| A.铵盐与碱的反应一般为放热反应 |
| B.化学反应一定既伴随着物质变化又伴随着能量变化 |
| C.反应物断旧键所吸收的能量高于生成物形成新键所放出的能量的反应为放热反应 |
| D.反应物所具有的总能量高于生成物所具有的总能量的反应为吸热反应 |
键能是指断开1mol共价键吸收的能量或形成1mol共价键放出的能量,已知H-H键能为436kJ/mol,H-Cl键能为431kJ/mol,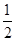 H2(g)+
H2(g)+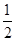 Cl2(g)=HCl(g) △H=-akJ/mol则Cl-Cl键能为
Cl2(g)=HCl(g) △H=-akJ/mol则Cl-Cl键能为
| A.(2a-426)kJ/mol | B.(426-a)kJ/mol |
| C.(426-2a)kJ/mol | D.(426+a)kJ/mol |
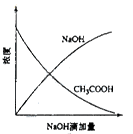
下列各图有关量的变化趋势中错误的是
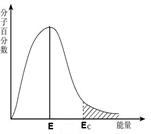
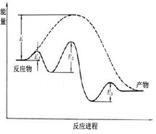
A B C D
| A.图A为向盐酸中滴加NaOH发生中和反应过程中溶液温度的变化趋势 |
| B.图B为向醋酸中滴加NaOH发生中和反应过程中各物质浓度的变化趋势 |
| C.图C中能量≥Ec的分子称为活化分子,E为分子平均能量,则活化能为Ec-E |
| D.图D为未加入催化剂和加入催化剂的反应进程中的能量变化 |
已知在25℃时:2C(s)+O2(g)=2CO(g) △H1=-222kJ/mol
2H2(g)+O2(g)=2H2O(g) △H2=-484kJ/mol
C(s)+O2(g)=CO2(g) △H3=-394kJ/mol
则25℃时,CO(g)+H2O(g)=CO2(g)+H2(g)的反应热△H4为
| A.-82kJ/mol | B.-41kJ/mol | C.-312kJ/mol | D.+82kJ/mol |
下列说法中正确的是
| A.同温同压下,H2(g)+Cl2(g)= 2HCl(g)在光照条件下和点燃条件下的ΔH不同 |
| B.常温下,2A(s)+B(g)= 2C(g)+D(g)不能自发进行,则该反应焓变一定大于零 |
| C.1mol硫酸与1molBa(OH)2完全中和所放出的热量为中和热 |
| D.在25℃、101KPa时,2mol S的燃烧热是1mol S的2倍 |
已知: 2H2(g) + O2(g) = 2H2O (l) △H=─571.6 kJ/mol,
CO(g)+ O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
某H2和CO的混合气体完全燃烧时放出113.74kJ 热量,同时生成 3.6 g液态水,则原混合气体中H2和CO的物质的量之比为
| A.2:1 | B.1:2 | C.1:1 | D.2:3 |
未来新能源的特点是资源丰富、对环境污染小,且可以再生。下列属于未来新能源的是
①天然气 ②煤 ③氢能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能
| A.①②③④ | B.③⑤⑥⑦ | C.④⑤⑥⑦ | D.①③⑤⑥ |
下列说法或表示方法中,正确的是
| A.等质量的硫蒸气和硫黄分别完全燃烧,前者放出的热量多 |
| B.a ℃、b kPa下,将0.5 mol O2和1.5 mol H2置于密闭容器中充分反应生成H2O(g),放热c kJ,其热化学方程式为2H2(g)+O2(g)=2H2O(g) ΔH=-2c kJ·mol-1 |
| C.常温常压下,2.8 g CO气体完全燃烧放出的热量为28.26 kJ,则表示CO燃烧热的热化学方程式为2CO(g)+O2(g)=2CO2(g) ΔH=-565.2 kJ·mol-1 |
| D.稀硫酸溶液与稀NaOH溶液反应的中和热为57.3 kJ·mol-1,则稀醋酸溶液与稀NaOH溶液反应的热化学方程式可表示为CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 |
盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以用盖斯定律间接求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出x kJ热量;已知每摩尔单质碳完全燃烧生成CO2放出热量为y kJ,则1 mol C与O2反应生成CO的反应热ΔH为
| A.-y kJ·mol-1 | B.-(10x-y)kJ·mol-1 |
| C.-(5x-0.5y)kJ·mol-1 | D.+(10x-y)kJ·mol-1 |