题目内容
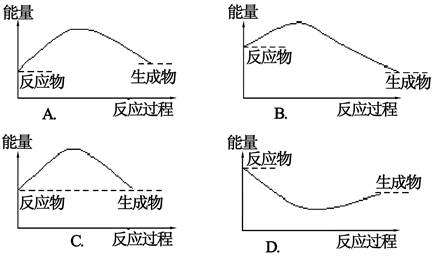
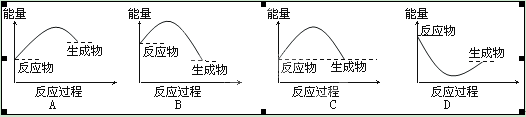
下列关于化学反应与能量的说法正确的是
| A.铵盐与碱的反应一般为放热反应 |
| B.化学反应一定既伴随着物质变化又伴随着能量变化 |
| C.反应物断旧键所吸收的能量高于生成物形成新键所放出的能量的反应为放热反应 |
| D.反应物所具有的总能量高于生成物所具有的总能量的反应为吸热反应 |
B
解析试题分析:A.错 铵盐与碱的反应一般为吸热反应。B 对 有新物质生成的反应才是化学反应,并且每个化学反应都伴随着能量的变化。C.错 反应物断旧键需吸热,生成物形成新键放热,前者大于后者,应为吸热反应。D.错 反应物所具有的总能量高于生成物所具有的总能量的反应为放热反应。
考点:化学反应热。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列装置工作时实现化学能转化为电能的是
| A.干电池 | B.光伏电池 | C.离子交换膜电解槽 | D.风力发电机 |
已知:H2(g)+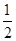 O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1 ② O2(g)=O2(l) ΔH3=-6.84 kJ·mol-1 ③
H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1 ④
下列说法正确的是
| A.上述四个反应都是吸热反应 |
| B.1 mol液态H2的能量大于1 mol气态H2的能量 |
| C.H2的燃烧热(ΔH)为-285.8 kJ·mol-1 |
D.火箭中液氢燃烧的热化学方程式为H2(l)+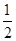 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 |
已知: 2H2(g) + O2(g) = 2H2O (l) △H=─571.6 kJ/mol,
CO(g)+ O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
某H2和CO的混合气体完全燃烧时放出113.74kJ 热量,同时生成 3.6 g液态水,则原混合气体中H2和CO的物质的量之比为
| A.2:1 | B.1:2 | C.1:1 | D.2:3 |
下列说法正确的是
| A.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H相同 |
| B.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 |
| C.已知:①2H2(g) +O2(g) =2H2O(g) △H="-a" kJ·mol-1,②2H2(g)+O2 (g)= 2H2O(1)△H="-b" kJ·mol-1,则a>b |
| D.已知:①C(s,石墨)+O2 (g)=CO2(g)△H="-" 393.5kJ·mol-1,②C(s,金刚石)+O2(g)=CO2 (g)△H="-" 395.0 kJ·mol-1,则C(s,石墨)=C(s,金刚石)△H=" -1.5" kJ·mol-1 |
已知反应:
①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列结论正确的是( )
| A.碳的燃烧热等于110.5 kJ·mol-1 |
| B.2mol C(s)在1 mol O2(g)燃烧,放出221 kJ热量 |
| C.1L0.1 mol/L H2SO4溶液与1L0.1 mol/L NaOH溶液反应,放出5.73 kJ热量 |
| D.pH=3的醋酸与pH=11的NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
在压强为2.20×104 kPa、温度达到374℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法不正确的是( )
| A.二氧化碳与超临界水作用生成汽油的反应,属于放热反应 |
| B.“水热反应”是一种复杂的物理化学变化 |
| C.火力发电厂可望利用废热,将二氧化碳转变为能源物质 |
| D.随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |