题目内容
已知: 2H2(g) + O2(g) = 2H2O (l) △H=─571.6 kJ/mol,
CO(g)+ O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
某H2和CO的混合气体完全燃烧时放出113.74kJ 热量,同时生成 3.6 g液态水,则原混合气体中H2和CO的物质的量之比为
| A.2:1 | B.1:2 | C.1:1 | D.2:3 |
C
解析试题分析:结合热化学方程式生成3.6g水时,消耗的氢气为0.2mol,同时放热57.16k J,则CO燃烧放热为113.74-57.16="56.58k" J,CO的物质的量为0.2mol,
考点:热化学方程式的计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生.下列属于未来新能源标准的是( )
①天然气 ② 生物质能 ③潮汐能 ④石油 ⑤太阳能 ⑥煤 ⑦风能 ⑧氢能
| A.①②③④ | B.②③⑤⑦⑧ | C.⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |
下列有关化学反应与能量的说法正确的是
| A.酸碱中和是放热反应 |
| B.炭在二氧化碳气体中灼烧发生的反应属于放热反应 |
| C.原子间形成化学键时需吸收能量 |
| D.化学反应过程中,化学能一定全部转化成热能 |
H2与O2发生反应的过程用模型图示如下(“—”表示化学键):下列说法不正确的是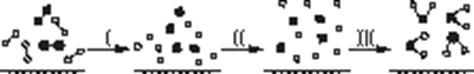
| A.过程Ⅰ是吸热过程 |
| B.过程Ⅲ一定是放热过程 |
| C.该反应过程所有旧化学键都断裂,且形成了新化学键 |
| D.该反应的能量转化形式只能以热能的形式进行 |
下列关于化学反应与能量的说法正确的是
| A.铵盐与碱的反应一般为放热反应 |
| B.化学反应一定既伴随着物质变化又伴随着能量变化 |
| C.反应物断旧键所吸收的能量高于生成物形成新键所放出的能量的反应为放热反应 |
| D.反应物所具有的总能量高于生成物所具有的总能量的反应为吸热反应 |
下列叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.反应是放热反应还是吸热反应,由生成物与反应物的焓值差决定 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。对该反应的有关叙述正确的是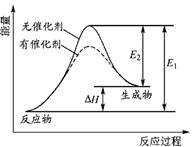
| A.该反应的正反应为吸热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂不能降低反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496 kJ,水蒸气1molH-O键形成时放出热量463 kJ,则氢气中1molH-H键断裂时吸收热量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
已知:常温下,0.01 mol/L MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
| A.-69.4 kJ·mol-1 | B.-45.2 kJ·mol-1 |
| C.+69.4 kJ·mol-1 | D.+45.2 kJ·mol-1 |