已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
以下反应属于吸热反应的是:
| A.锌与稀硫酸的反应 | B.氯化铵与氢氧化钡晶体反应 |
| C.煤的燃烧 | D.氢氧化钠与盐酸的反应 |
已知:①101 kPa时,2C(s)+O2(g)==="2CO(g)" ΔH=-221 kJ/mol;
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol。
下列结论正确的是
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
已知:
①I2(g)+H2(g)  2HI(g) ΔH1=-9.48 kJ/mol
2HI(g) ΔH1=-9.48 kJ/mol
②I2(s)+H2(g)  2HI(g) ΔH2=+26.48 kJ/mol
2HI(g) ΔH2=+26.48 kJ/mol
下列判断正确的是
| A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ |
| B.I2(g)===I2(s) ΔH=-17.00 kJ/mol |
| C.固态碘的稳定性比气态碘的稳定性高 |
| D.1 mol固态碘和1 mol气态碘分别与氢气完全反应,前者断裂的I—I键更多 |
有关热化学方程式书写与对应表述均正确的是
| A.稀醋酸与0.1 mol·L-1 NaOH溶液反应:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1 |
| B.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量,则Fe(s)+S(s)==="FeS(s)" ΔH=-95.6 kJ·mol-1 |
| C.氢气的燃烧热为285.5 kJ·mol-1,则水电解的热化学方程式为2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 |
| D.已知2C(s)+O2(g)==="2CO(g)" ΔH=-221 kJ·mol-1,则可知C的燃烧热为110.5 kJ·mol-1 |
烷烃分子中去掉2个氢原子形成一个双键是吸热反应,1,3—环己二烯失去2个氢原子生成苯是放热反应。下列说法正确的是
| A.1,3—环己二烯加氢是吸热反应 | B.1,3—环己二烯比苯稳定 |
| C.苯比1,3—环己二烯稳定 | D.苯加氢生成环己烷是吸热反应 |
已知热化学方程式N2(g) + 3H2(g)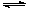 2NH3(g) + Q kJ(Q>0),下列说法中,正确的是
2NH3(g) + Q kJ(Q>0),下列说法中,正确的是
| A.1mol N2(g)和3mol H2(g)具有的能量之和低于2 mol NH3(g)具有的能量 |
| B.将1mol N2 (g)和3mol H2 (g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| C.升高温度,平衡向逆反应方向移动,上述热化学方程式中的Q值减小 |
| D.将一定量N2(g)和H2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有3mol H2被氧化 |
已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1 kJ,又知胆矾分解的热化学方程式为:CuSO4·5H2O(s)  CuSO4(s)+5H2O(l) ΔH=+Q2 mol·L
CuSO4(s)+5H2O(l) ΔH=+Q2 mol·L 则Q1和Q2的关系为( )
则Q1和Q2的关系为( )
| A.Q1<Q2 | B.Q1>Q2 | C.Q1=Q2 | D.无法确定 |
下列有关中和热的说法正确的是( )
| A.表示中和热的热化学方程式:H+(l)+OH-(l)=H2O(l) ΔH=-57.3 kJ/mol |
| B.准确测量中和热的实验过程中,至少需测定温度4次 |
| C.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 |
| D.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol,则该反应的中和热为114.6 kJ/mol |
