金刚石和石墨是碳元素的两种结构不同的单质.在101kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的能量.下列说法不正确的是( )
| A.石墨比金刚石稳定 |
| B.金刚石与石墨的性质相似 |
| C.1mol金刚石比1mol石墨的总能量高 |
| D.1mol石墨和金刚石完全燃烧时释放的能量石墨比金刚石少 |
下列说法或表示方法正确的是( )
| A.等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B.由C(石墨)→C(金刚石) ΔH=+11.9kJ·mol-1可知,金刚石比石墨稳定 |
| C.在25℃,101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| D.H+(aq)+OH-(aq)= H2O(l) ΔH=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量等于57.3kJ |
根据表中的信息判断下列说法正确的是( )。
| 物质 | 金刚石 | 石墨 |
| 外观 | 无色,透明固体 | 灰黑,不透明固体 |
| 熔点 | ? | ? |
| 燃烧热/(kJ·mol-1) | 395.4 | 393.5 |
 O2(g)=CO(g) ΔH=-393.5kJ·mol-1
O2(g)=CO(g) ΔH=-393.5kJ·mol-1B.由表中信息知C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1
C.由表中信息可得如图所示的图像

D.由表中信息可推知相同条件下金刚石的熔点高于石墨的熔点
已知下列反应的热化学方程式:6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) △H1
2 H2(g)+O2(g)=2H2O(g) △H2
C(s)+O2(g)=CO2(g) △H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
| A.12△H3+5△H2-2△H1 | B.2△H1-5△H2-12△H3 |
| C.12△H3-5△H2-2△H1 | D.△H1-5△H2-12△H3 |
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-55.6kJ·mol-1。则HCN在水溶液中电离的ΔH等于( )
| A.+43.5kJ·mol-1 | B.-43.5kJ·mol-1 | C.+67.7kJ·mol-1 | D.-67.7kJ·mol-1 |
已知反应A+B=C+D的能量变化如右图所示,下列说法正确的是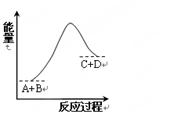
| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |
Ⅰ下列描述中正确的是( )
| A.CS2为V形的极性分子 |
B.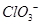 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.SF6中有6对完全相同的成键电子对 |
D.SiF4和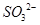 的中心原子均为sp3杂化 的中心原子均为sp3杂化 |
(1)Ni原子的核外电子排布式为__________________________________;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,
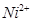 和
和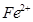 的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);
的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);(3)NiO晶胞中Ni和O的配位数分别为_________________、_________________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_________________;

(5)丁二酮肟常用于检验
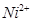 :在稀氨水介质中,丁二酮肟与
:在稀氨水介质中,丁二酮肟与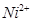 反应可生成鲜红色沉淀,其结构如右上图所示。
反应可生成鲜红色沉淀,其结构如右上图所示。①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是_________________。氮镍之间形成的化学键是_________________;
②该结构中,氧氢之间除共价键外还可存在_________________键;
③该结构中,碳原子的杂化轨道类型有_________________。
某金属(A)在TK以下晶体的基本结构单元如左下图所示,T K以上转变为右下图所示结构的基本结构单元,在两种晶体中最邻近的A原子间距离相同

(1)在T K以下的纯A晶体中,与A原子等距离且最近的A原子数为______个;在T K以上的纯A晶体中,与A原子等距离且最近的A原子数为___________;
(2)纯A晶体在晶型转变前后,二者基本结构单元的边长之比为(TK以上与TK以下之比)___________。
(3)左上图的的堆积方式为 , 经测定其结构和性质参数如下表所示
| 金属 | 相对原子质量 | 分区 | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
| Na | 22.99 | s区 | 0.960 | 108.4 |
| A | 60.20 | d区 | 7.407 | 7735 |
则A原子的原子半径为 pm,试解释该晶体原子化热很高的原因 。
(已知
 ,7.407≈
,7.407≈ ,1pm=10
,1pm=10 m)
m) 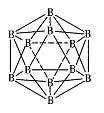 ③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。