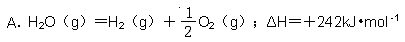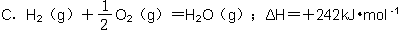题目内容
下列说法或表示方法正确的是( )
| A.等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B.由C(石墨)→C(金刚石) ΔH=+11.9kJ·mol-1可知,金刚石比石墨稳定 |
| C.在25℃,101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| D.H+(aq)+OH-(aq)= H2O(l) ΔH=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量等于57.3kJ |
C
解析试题分析:A、硫蒸汽所含能量比硫固体高,所以,等物质的量的硫蒸汽和硫固体分别完全燃烧,前者放出热量多,故A错误;B、从热化学方程式看,石墨能量低,物质所含能量越低越稳定,故B错误;C、2g氢气是1mol,热化学方程式应为:2H2(g)+O2(g)═2H2O(l) △H=-571.6kJ?mol-1,故C正确;D、浓硫酸溶解时放热,所以,将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ,故D错误,故选:C。
考点:考查反应热的有关判断、计算以及应用等

练习册系列答案
相关题目
下列对各组物质性质的比较中,正确的是
| A.第一电离能:Na<Mg<Al |
| B.熔点:金刚石>晶体硅>碳化硅 |
| C.硬度:Li>Na>K |
| D.空间利用率:六方密堆<面心立方<体心立方 |
下列能源中属于二次能源的是( )
| A.天然气 | B.电力 | C.原煤 | D.石油 |
已知下列反应的热化学方程式为:
(1)C(s)+O2(g)=CO2(g) ΔH 1=-393.5kJ/mol
(2)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
(3)H2(g)+ O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热ΔH为
| A.+488.3 kJ/mol | B.-488.3 kJ/mol | C.-244.15 kJ/mol | D.+244.15 kJ/mol |
已知298K时下述反应的有关数据:C(s)+1/2 O2(g)=CO(g) △H1 = -110.5kJ·mol-1
C(s)+O2 (g)=CO2(g), △H2= -393.5kJ/mol 则 C(s)+CO2(g)="2CO(g)" 的△H为
| A.283. kJ·mol-1 | B.+172.5 kJ·mol-1 |
| C.-172.5 kJ·mol-1 | D.-504 kJ·mol-1 |

 (1)A的元素符号是 ;E在元素周期表中的位置是 ,它的+2价离子的电子排布式为 。
(1)A的元素符号是 ;E在元素周期表中的位置是 ,它的+2价离子的电子排布式为 。 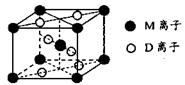
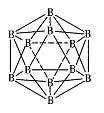 ③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。