中心原子采取sp2杂化的是 ( )
| A.NH3 | B.BCl3 | C.PCl3 | D.H2O |
下列说法正确的是( )
| A.CHCl3是正四面体形 |
| B.H2O分子中氧原子为sp2杂化,其分子几何构型为V形 |
| C.二氧化碳中碳原子为sp杂化,为直线形分子 |
D.NH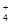 是三角锥形 是三角锥形 |
下列物质的分子中,既有σ键又有π 键的是( )
| A.C2H6 | B.HClO | C.CH4 | D.CO2 |
下列叙述中正确的是
| A.离子化合物熔融状态下一定导电 |
| B.金属元素跟非金属元素化合时都能形成离子键 |
| C.离子化合物中的阳离子只能是金属离子,酸根离子中不能含有金属元素 |
| D.离子化合物中不一定含有离子键,含共价键的化合物不一定是共价化合物 |
化学变化的实质是旧的化学键断裂、新的化学键形成。据此判断下列变化是化学变化的是
| A.固体氯化钠溶于水 | B.冰经加热变成水蒸气 |
| C.氯化铵受热分解生成氯化氢和氨气 | D.氯化氢溶于水 |
下列说法中错误的是
| A.CO2、SO3都是极性分子 |
| B.KF是离子化合物,HF为共价化合物 |
| C.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
| D.PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是
| A.CS2是V形分子 | B.SnBr2键角大于120° |
| C.BF3是三角锥形分子 | D.NH4+键角等于109.5° |
正硼酸(H3BO3)是一种层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。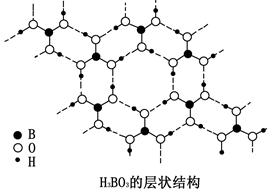
下列有关说法正确的是
| A.正硼酸晶体属于原子晶体 | B.H3BO3分子的稳定性与氢键有关 |
| C.分子中硼原子最外层为8电子稳定结构 | D.含1molH3BO3的晶体中有3mol氢键 |
下列关于丙烯(CH3—CH=CH2)的说法正确的是
| A.一个丙烯分子中有8个σ键和1个π键 |
| B.丙烯分子中3个碳原子可能在同一直线上 |
| C.丙烯分子中3个碳原子都是sp3杂化 |
| D.丙烯分子中不存在非极性键 |
下列各组分子中,均含有非极性键且属于非极性分子的是
| A.C2H2、NH3 | B.Cl2、C2H4 | C.CO2、H2S | D.CH4、H2O2 |