下列叙述中,正确的是
| A.同周期元素中,ⅦA族元素的原子半径最大 |
| B.ⅥA族元素的原子,其半径越大,越容易得到电子 |
| C.室温时,0族元素的单质都是气体 |
| D.元素周期表中,从ⅢB到ⅡB这10个纵行的元素都是副族元素 |
下列各组粒子所含电子数目相同的是
| A.NH4+、OH-、H3O+ |
| B.Na+、Mg2+、S2- |
| C.F-、NH2-、Cl- |
| D.Li+、Na+、K+ |
铋(Bi)在医药方面有重要应用。 下列关于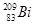 和
和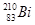 的说法正确的是
的说法正确的是
A.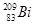 和 和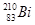 都含有83个中子 都含有83个中子 |
B.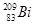 和 和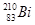 互为同位素 互为同位素 |
C.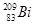 和 和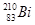 的核外电子数不同 的核外电子数不同 |
D.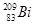 和 和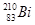 分别含有126和127个质子 分别含有126和127个质子 |
下列有关原子结构和元素周期律的表述,正确的是( )
①原子序数为16的元素的最高化合价为+4
②IA族元素是同周期中失电子能力最强的元素
③第2周期IVA族元素的原子核电荷数和中子数一定为6
④原子序数为13的元素位于元素周期表的第3周期III族
| A.①② | B.①③ | C.②④ | D.③④ |
X、Y、Z为短周期元素,原子序数依次增大。X原子的最外层电子数是Y原子最外层电子数的2倍,质子数比Y少5,X和Z在同一主族。下列叙述不正确的是( )
| A.原子半径:Y>Z |
| B.X元素的一种单质可用于消毒杀菌 |
| C.Y的氧化物是工业制取Y单质的主要原料 |
| D.Z的单质在氧气中点燃可生成两种酸性氧化物 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)2 |
短周期元素的离子aW2+、bX+、cY2-、dZ-具有相同的电子层结构,下列推断正确的是
| A.热稳定性:H2Y<HZ | B.原子半径:W>X>Z>Y |
| C.离子半径:W2+>Y2- | D.碱性:XOH<W(OH)2 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)2 |
A和B是短周期的两种元素,它们的离子A-和B2+具有相同的核外电子层结构,下列说法中正确的是。
| A.原子序数A>B | B.电子总数A>B |
| C.原子半径A>B | D.离子半径A->B2+ |